
题目列表(包括答案和解析)
| 实验步骤 | 所用实验试剂及操作 |
① ① |
取少量样品放入试管甲里 |
⑥ ⑥ |
再向溶液里滴加几滴AgNO3溶液 |
④ ④ |
过滤,取少量滤液盛在试管乙里 |
② ② |
向试管里加入适量的蒸馏水,振荡 |
⑤ ⑤ |
滴入几滴酚酞溶液 |
③ ③ |
(1) 向试管甲中加入适量的硝酸钡溶液 向试管甲中加入适量的硝酸钡溶液 |
⑦ ⑦ |
(2) 向试管乙中加入适量的稀硝酸 向试管乙中加入适量的稀硝酸 |
Ⅰ.(6分)某同学做“铝热反应”的实验。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3
熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | —— |
(1)铝热反应方程式为 .
(2)下列能与Al发生铝热反应的有 。(填序号)
A、MnO2 B、Na2O C、MgO D、FeO
(3)据上表数据该同学推测,铝热反应所得到的熔融物应是铁铝合金。若证明上述所得的块
状熔融物中含有金属铝,所用试剂是 ,该试剂溶质的电子式为 。
Ⅱ.(6分)某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的实验仪器有
_______________等。(填代号,下同)
A、试管 B、坩埚 C、烧杯 D、三角架
E、泥三角 F、洒精灯 G、铁架台 H、量筒
(2)第2步:Iˉ溶液的获取。操作是将灰烬转移到烧杯中,加适量蒸馏水,用玻棒充分
搅拌,煮沸,冷却,________。(填分离方法)
(3)第3步:氧化。取(2)中溶液少量依次加入合适的试剂。下列氧化剂最好选_________。
A、浓硫酸 B、新制氯水 C、KMnO4溶液 D、H2O2
(4)第4步:碘单质的检验。操作是取少量第3步的溶液,滴加_______溶液,证明海
带中含碘。
(4分)I. 下列实验操作或对实验事实的描述不正确的是 (填序号)
①分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
②向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
③石油的分馏实验中,需将温度计的水银球插入液面以下以控制液体温度
④用瓷坩埚熔化各种钠的化合物
⑤测溶液大致的pH:用玻璃棒蘸取溶液滴在湿润的pH试纸上,与标准比色卡对照
⑥向NaOH溶液中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加NaOH溶液现象不同
⑦可用饱和碳酸氢钠溶液除去二氧化碳中混有的少量二氧化硫
II. (6分)某同学设计了如图所示的套管实验装置(部分装置未画出)来制备SO2并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4。回答下列问题: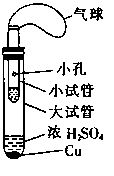
(1)写出制取SO2的化学方程式: 。
(2)该反应中浓H2SO4表现的化学性质有 。
(3)该同学利用实验现象来检验SO2的还原性,则选用的试剂为 。
A.双氧水(H2O2) B.品红溶液 C.酸性高锰酸钾溶液
检验SO2还原性的试管中的现象为 。
(6分) 某同学进行如下实验,探究化学反应中的能量变化。

通过实验测出,反应前后①烧杯中的温度升高,②烧杯中的温度降低。由此判断NaOH溶液跟盐酸的反应是 (填 “吸热”或“放热”)反应,Ba(OH)2· 8H2O跟NH4Cl的反应是 (填“吸热”或“放热”)反应。反应①中反应物的总能量 填(“大于”、“小于”或“等于”)生成物的总能量。反应②中断开反应物中的化学键所吸收的能量 填(“大于”、“小于”或“等于”)形成生成物中的化学键所放出的能量。
(6分) 某同学欲配制250 mL 2 mol·L-1 的碳酸钠溶液,并进行有关实验。请回答下列问题:
(1)需称量无水碳酸钠的质量 g。
(2)配制该碳酸钠溶液时使用的仪器除天平(带砝码)、烧杯、玻璃棒外,还必须用到的仪器有 、 等。
(3)取所配制的碳酸钠溶液125 mL,向其加入125 mL 3mol·L-1 的硫酸溶液,待充分反应后,生成的气体在标准状况下所占的体积为(假设产生的气体全部逸出) ;设反应后溶液的体积为250mL,则反应后溶液中Na+的物质的量浓度为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com