为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1).已知热化学方程式:
①.Fe
2O
3(s)+3CO
(g)=2Fe
(s)+3CO
2(g)△H=-25kJ/mol
②.3Fe
2O
3(s)+CO
(g)=2Fe
3O
4(s)+CO
2(g)△H=-47kJ/mol
③.Fe
3O
4(s)+CO
(g)=3FeO
(s)+CO
2(g)△H=+19kJ/mol
写出FeO
(s)被CO
(g)还原成Fe
(s)和CO
2(g)的热化学方程式
FeO(s)+CO(g)=Fe(s)+C02(g)△H=-11kJ/mol.
FeO(s)+CO(g)=Fe(s)+C02(g)△H=-11kJ/mol.
.
(2).由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.
| 化学键 |
H-H |
N-H |
N≡N |
| 键能/kJ?mol-1 |
436 |
391 |
946 |
已知反应N
2(g)+3H
2 (g)?2NH
3(g)△H=a kJ/mol.试根据表中所列键能数据计算a为
-92
-92
.
(3).依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C
(s,石墨)+O
2 (g)=CO
2(g)△H
1=+393.5kJ/mol
2H
2(g)+O
2 (g)=2H
2O
(l)△H
2=-571.6kJ/mol
2C
2H
2(g)+5O
2 (g)=4CO
2 (g)+2H
2O
(l)△H
3=-2599kJ/mol
根据盖斯定律,计算298K时反应2C
(s,石墨)+H
2(g)=C
2H
2(g)的焓变:△H=
+226.7KJ/mol
+226.7KJ/mol
.

 二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚.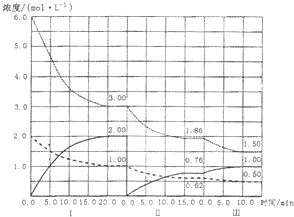
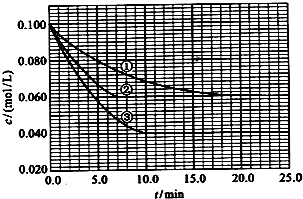
 已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与P、T的关系如图,根据图示可以得出的正确结论是( )
已知反应mA(g)+nB(g)?xC(g)+yD(g),A的转化率RA与P、T的关系如图,根据图示可以得出的正确结论是( )