
题目列表(包括答案和解析)

已知:
①FeS不溶解于水;
②实验室制取H2S、SO2气体的原理是:
FeS+H2SO4=FeSO4+H2S↑
Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;
③硫化氢与二氧化硫气体相遇会发生反应:2H2S+SO2=3S+2H2O。
根据下图中A~D的实验装置和试剂进行实验,回答下列问题:

(1)装置A是由双孔塞、玻璃导管及 和 组装起来的。
(2)组装一套制取SO2气体的装置,并证明SO2既有氧化性、又有还原性和漂白性。
①按实验装置连接顺序,把a![]() f各导管口连接起来,正确的顺序有 。
f各导管口连接起来,正确的顺序有 。
A.befcda B.adcefb C.acdfeb D.acdefb
②若C装置中的溶液为 ,反应后该溶液变为无色,说明SO2具有还原性;? ③若C装置中的溶液为 ,反应后该溶液变为无色,说明SO2具有漂白性;
④当D中产生 现象时,说明SO2具有氧化性;
(3)D装置烧杯中NaOH溶液的作用 。

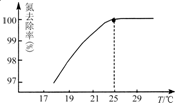 氮可以形成多种化合物,如NH3、N2H4、HCN、NH4NO3等.
氮可以形成多种化合物,如NH3、N2H4、HCN、NH4NO3等.- 4 |
- 4 |
2- 4 |
2- 8 |
2- 8 |
+ 4 |
+ 4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com