
题目列表(包括答案和解析)
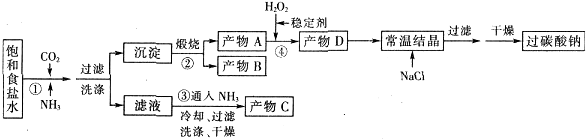
过碳酸钠(Na2CO3·3H2O2),有固体双氧水的俗称,该晶体具有Na2CO3和H2O2的双重性质,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,过碳酸钠的某生产流程如下图所示。
已知:2Na2CO3+3H2O2=2Na2CO3·3H2O △H<0;回答下列问题: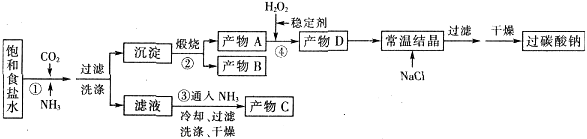
(1)下列物质可使过碳酸钠较快失效的是(填序号)_________。
| A.FeCl3溶液 | B.H2S | C.稀硫酸 | D.NaHCO3溶液 |
| T/℃ | 活性氧百分含量 | 产率 |
| 5~10 | 13.94 | 85.49 |
| 10~15 | 14.02 | 85.78 |
| 15~20 | 15.05 | 88.38 |
| 20~25 | 14.46 | 83.01 |
 、
、
| A.FeCl3溶液 | B.H2S | C.稀硫酸 | D.NaHCO3溶液 |
| T/℃ | 活性氧百分含量 | 产率 |
| 5~10 | 13.94 | 85.49 |
| 10~15 | 14.02 | 85.78 |
| 15~20 | 15.05 | 88.38 |
| 20~25 | 14.46 | 83.01 |
 、
、(08上海松江区模拟)过碳酸钠是由碳酸钠和过氧化氢复合形成的一种新型氧系漂白剂,具有碳酸钠和过氧化氢的双重性质,其分子式为2Na2CO3?3H2O2,已知过渡元素的金属离子可作为催化剂使之分解。
它的制备原理和湿法生产路线如下:2Na2CO3 + 3H2O2 → 2 Na2CO3?3H2O2
 |
回答下列问题:
(1)反应控制在0~5℃条件下进行,其主要原因是 ,流程中的“分离”指的是实验操作中的 ;
(2)工业碳酸钠中一般含有少量锰、铜等金属离子(用M2+表示),加入稳定剂的作用是将M2+沉淀而除去,M2+对产品的不良影响是 ,
若加入的稳定剂是Na2SiO3,反应的离子方程式为 ;
(3)加入的食盐为盐析剂,其原理是降低过碳酸钠的溶解度使之析出。盐析是物理变化还是化学变化? ;
(4)过碳酸钠在生产上的应用是利用它分解所释放的H2O2。以铜为原料用H2O2氧化是工业上制胆矾的方法之一。做法是:
将铜丝放到一定量的稀硫酸中,控温在50℃,加入一定量的H2O2溶液,反应0.5h后,升温到60℃,再持续反应1 h,过滤后取滤液,再经过“某些操作”、减压抽滤,用少量95%的酒精淋洗后晾干,可得CuSO4?5H2O。
①在反应中,起氧化作用的是H2O2,写出H2O2在稀硫酸中氧化单质铜的化学反应方程式 ;
②处理滤液时的“某些操作”指的是 ;
③晶体采用酒精淋洗的优点是 。
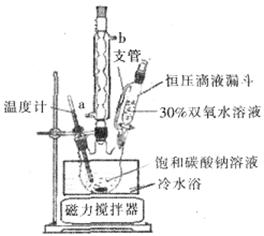
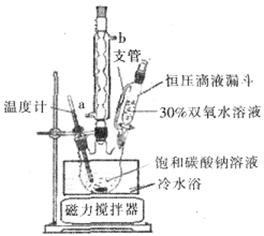
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,该晶体具有Na2CO3和H2O2的双重性质。利用图-2装置制备过碳酸钠,在冷水浴中充分反应后,按图-1流程可获得过碳酸钠产品。
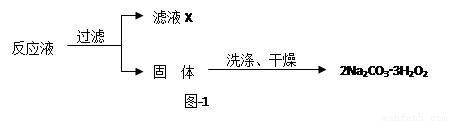
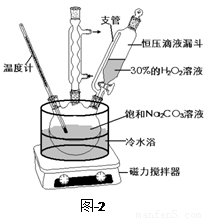
(1)恒压滴液漏斗中支管的作用是 。
(2)制备过碳酸钠的关键是 。
(3)如果配制过碳酸钠的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因(写出其中一种即可,用方程式表示)。________________________________;
(4)某化学学习小组为了定性探究铁离子对这种新型漂白剂的不良影响,取该漂白剂100mL,加入25g FeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.1mol/LNaOH溶液、8.0mol/LNaOH溶液、澄清石灰水、0.01mol/LKMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2; 假设2:气体是______________; 假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论:
|
实验步骤 |
预期现象与结论 |
|
将气体依次通入盛有_______、________的洗气瓶中,________________________。 |
①________________________ ②________________________ ③________________________ |
过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,该晶体具有Na2CO3和H2O2的双重性质。利用图-2装置制备过碳酸钠,在冷水浴中充分反应后,按图-1流程可获得过碳酸钠产品。

(1)恒压滴液漏斗中支管的作用是 。
(2)制备过碳酸钠的关键是 。
(3)如果配制过碳酸钠的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至完全失去杀菌作用。试分析其中的原因(写出其中一种即可,用方程式表示)。________________________________;
(4)某化学学习小组为了定性探究铁离子对这种新型漂白剂的不良影响,取该漂白剂100mL,加入25g FeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.1mol/LNaOH溶液、8.0mol/LNaOH溶液、澄清石灰水、0.01mol/LKMnO4溶液、BaCl2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2; 假设2:气体是______________; 假设3:气体是CO2。
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象与结论:
| 实验步骤 | 预期现象与结论 |
| 将气体依次通入盛有_______、________的洗气瓶中,________________________。 | ①________________________ ②________________________ ③________________________ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com