
题目列表(包括答案和解析)
(8分)①用0.1mol/L的盐酸滴定未知浓度的NaOH溶液 ,下列操作使滴定结果偏低的
是 (填序号)
(1)滴定前,在用蒸馏水洗涤滴定管后,未用标准液润洗。
(2)滴定前,滴定管尖端有气泡,滴定后气泡消失。
(3)滴定前,用待测液润洗锥形瓶。
(4)读取标准液的刻度时,滴定前平视,滴定后俯视。
(5)滴定后,滴定管尖端挂有液滴未滴入锥形瓶中。
(6)滴定过程中,锥形瓶振荡太剧烈,有少量溶液溅出。
(7)滴定过程中向锥形瓶内加入少量蒸馏水。
(8)过早估计滴定终点。
②、正确书写电离方程式
H2SO3
Cu(OH)2
NaHCO3
乙酰水杨酸俗称阿司匹林,是一种历史悠久的解热镇痛药。合成原理是:

虚框中为提纯原理,是为了除去该反应的副产物:水杨酸酐、乙酰水杨酸水杨酯、乙酰水杨酸酐和聚合物等。水杨酸(熔点158℃)和乙酰水杨酸(熔点135℃)微溶于冷水、可溶于热水和乙酸乙酯。生产流程是:

(1)操作I、III的名称是 ;使用热水浴加热的原因是 。
(2)可以循环利用的是 ;固体2的成份是 。
(3)为了检验产品中是否含有水杨酸,并进行精制(除去产品中的其它反应物和副产物),进行以下操作,请完成下表:
|
序号 |
操作 |
现象 |
结论 |
|
检 验 |
取几粒产品晶体投入装适量热水的试管中,振荡 |
得无色溶液 |
|
|
向试管中滴入 溶液 |
. |
产品中有水杨酸 |
|
|
重 结晶 |
将粗产品溶于适量的水中,水浴加热,趁热过滤,将滤液 ,抽滤 |
有晶体析出 |
精产品 |
(4)用中和法测定产品纯度:
取a g产品溶解于V1 mL1mol/L的NaOH溶液中,加热使乙酰水杨酸水解,再用1 mol/L的盐酸滴定过量的NaOH,当滴定终点时消耗盐酸V2 mL;计算出产品纯度为 (只需列出计算表达式,不必化简。乙酰水杨酸分子量为180)。
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示。
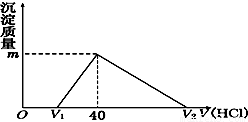
则下列选项正确的是
A.原合金质量为0.92 g
B.标准状况下产生氢气896 mL
C.图中m值为1.56 g
D.图中V2为60 mL
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL OH-浓度为1mol/L的溶液,以及一定量的H2;然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是
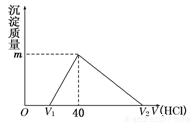
A.图中m值为1.56 g
B.标准状况下产生氢气896 mL
C.原合金质量为0.92 g
D.图中V2为60 mL
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL OH-浓度为1mol/L的溶液,然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com