
题目列表(包括答案和解析)
向一密闭容器中充入1mol A,2mol B,发生如下反应:A(g)+2B(g)![]() C(s)+3D(g), 在一定条件下达到平衡,测得混合气体D的浓度为l.4mol/L;
C(s)+3D(g), 在一定条件下达到平衡,测得混合气体D的浓度为l.4mol/L;
⑴若压缩容器增大压强,则逆反应的速率 ;容器中D的浓度 ;(填“增大”、“减小”或“不变”)
⑵温度升高,混合气体平均相对分子质量增大,则正反应 ;(填“吸热”或“放热”)
⑶在一体积可变的密闭容器中,充入0.8mol C,3.5mol D,若使D的浓度仍为l.4mol/L,则容器体积取值范围为 。
| A、用A的浓度变化表示的该反应平均速率为0.2 mol/(L?s) | B、平衡时A与B的转化率相等 | C、平衡时B的浓度为0.2 mol/L | D、其它条件不变,向容器中再加入1 mol C,达到新平衡时,C的体积分数不变 |
(12分)工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g)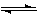 CH3OH(g) ΔH=-a kJ·mol-1
CH3OH(g) ΔH=-a kJ·mol-1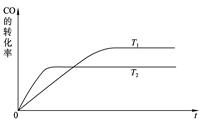
(1)上图是该反应在不同温度下CO的转化率随时间变化的曲线。
①a __0(填“>” “<” “=”)。
②下列说法正确的是_ _(填序号)。
a.1mol CO(g)和2mol H2(g)所具有的能量小于1mol CH3OH(g)所具有的能量
b.将1mol CO(g)和2mol H2(g)置于一密闭容器中充分反应后放出a KJ的热量
c.升高温度,平衡向逆反应移动,上述热化学方程式中的a值将减小
d.如将一定量CO(g) 和H2(g)置于某密闭容器中充分反应后放热aKJ,则此过程中有1molCO(g)被还原
(2)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示: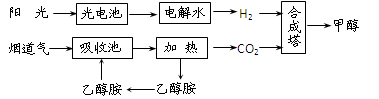
①该合成路线对于环境保护的价值在于_ _。
②15%~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2
吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
。
(3)甲醇燃料电池的工作原理如下左图所示。该电池工作时,c口通入的物质发生的电极
反应式为:_ _。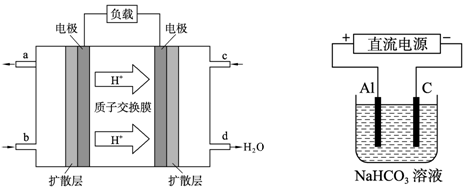
(4)以上述电池做电源,用上右图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
_ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com