
题目列表(包括答案和解析)
(本题共14分)5—氨基酮戊酸盐是一种抗肿瘤药,其合成路线如下: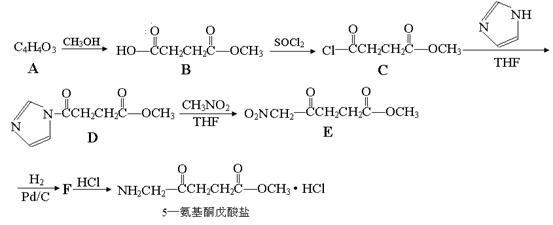
已知: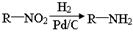
(1)已知A分子结构中有一个环,A不能使溴水褪色,且核磁共振氢谱图上只有一个峰,则A的结构简式为 。
(2)5—氨基酮戊酸盐中含氧官能团的名称是 ,C→D的反应类型为 。
(3)G是B的一种同分异构体,能与NaHCO3溶液反应,能发生银镜反应,1molG与足量金属Na反应能生成1molH2,且G分子中不含甲基,写出一种符合上述条件的G的结构简式 。
(4)写出D→E的反应方程式 。
(5)已知 ,请结合题中所给信息,写出由CH3CH2COOH、
,请结合题中所给信息,写出由CH3CH2COOH、 为原料合成
为原料合成 单体的合成路线流程图(无机试剂任选)。
单体的合成路线流程图(无机试剂任选)。
合成路线流程图示例如下: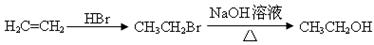
。
实验题:(本题共9分)某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:?
| A.在250 mL的容量瓶中配制250 mL烧碱溶液; | B.用碱式滴定管量取25.00 mL烧碱溶液于锥形瓶中并滴加几滴酚酞做指示剂;? | C.在天平上准确称取烧碱样品W g,在烧杯中用蒸馏水溶解; | D.将物质的量浓度为cmol/L的标准盐酸溶液装入酸式滴定管。调整液面记下开始读数为V1 mL;E.在锥形瓶下垫一张白纸,滴定最后一滴至红色刚好消失 为止,半分钟后不恢复红色,记下读数V2 mL。? 为止,半分钟后不恢复红色,记下读数V2 mL。? |
 2)观察滴定管里液面的高度时应注意: 。?
2)观察滴定管里液面的高度时应注意: 。?实验题:(本题共12分)
(1)用18.4mol/L的浓H2SO4配制100ml浓度为1mol/L的稀H2SO4,其操作可分为以下各步:
A.用量筒量取5.4ml浓H2SO4缓缓注入装有约50ml蒸馏水的烧杯中,并用玻璃棒搅拌;
B.用约30ml蒸馏水,分成3次洗涤烧杯和玻棒,将每次洗涤液都注入容量瓶中;
C.将稀释后的H2SO4小心倒入100ml容量瓶里;
D.检查100ml容量瓶口部是否会发生滴漏;
E、用量筒加蒸馏水至容量瓶中液面接近刻度2cm处;
F、盖紧瓶塞,反复颠倒振荡,摇匀溶液;
G、用胶头滴管向容量瓶里逐滴滴加蒸馏水至液面最低点和刻度线相平,试填空
①正确的操作顺序为(用字母填写) 。
②进行A步操作时,应选择下列量器 (填序号)
a、10ml量筒 b、50ml量筒 c、100ml量筒
③如果对装有浓H2SO4的量筒读数如右图所示,配制的稀H2SO4的浓度
将 (偏高、偏低、无影响)
④进入A步操作后,必须 后才能进行C操作。
(2)只从下列试剂中选择实验所需的试剂,采用两种不同的方法区分0.1mol/L的H2SO4和0.01mol/LH2SO4溶液,简述其操作过程:
试剂:紫色石蕊试液、酚酞试液、甲基橙试液、蒸馏水、BaCl2溶液、pH试纸、0.1mol/L Na2S2O3溶液
方法一:
。
方法二:
。
(每空2分,共10分。)
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。
完成下列各题:
(1) 正四面体烷的二氯取代产物有________种。
正四面体烷的二氯取代产物有________种。
(2)关于乙烯基乙炔分子的说法错误 的是________。
的是________。
a.能使酸性KMnO4溶液褪色
b.1 mol乙烯基乙炔能与3 mol Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举一例)________________。
(4)写出与环辛四烯互为同分异构体且属于芳香烃的物质发生加聚反应的反应方程式_______________。
(5)乙烯基乙炔可与HCl反应生成2-氯-1,3-丁二烯,写出2-氯-1,3-丁二烯加聚反应的反应方程式_______________。
(方程式2分,(4)题2分,其余每空1分,共8分)某地有一池塘,生长着丰富的水生植物和多种鱼、虾。后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡。根据题意回答下列问题:
(1)从生态平衡角度看,池塘这种变化说明了 。
(2)造成这种变化的原因是 。
(3)经检验,污水中含有0.012mol/L的游离溴,可用亚硫酸钠除去污水中的溴,请写出其化学方程式: 。
(4)处理10L这种污水需加入0.05mol/L的亚硫酸钠 升才能将溴全部除去。
(5)要使池塘恢复本来面目,首先要解决的问题是______________,首先要恢复的生物是______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com