
题目列表(包括答案和解析)
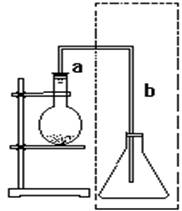
(共15分)下图是实验室制取溴苯的装置。填写以下内容:
(1)写出反应的化学方程式
(2)导管a段的作用 。导管b段末端跟锥形瓶里液面保持一段距离的目的是____________________,若锥形瓶内盛硝酸银溶液,图中虚线方框部分的作用
。
(3)反应后不久导管b出口可见到什么现象 。
若锥形瓶内盛硝酸银溶液,反应后出现淡黄色,______(填“能”或“不能”)证明苯与溴单质发生取代反应,这是因为___________________________________
(4)反应得到的溴苯呈______色,这是因为 ;为除去混入溴苯中的溴,可加入_____________试剂,用 方法分离。
(共15分)下图是实验室制取溴苯的装置。填写以下内容:
(1)写出反应的化学方程式
(2)导管a段的作用 。导管b段末端跟锥形瓶里液面保持一段距离的目的是____________________,若锥形瓶内盛硝酸银溶液,图中虚线方框部分的作用
。
(3)反应后不久导管b出口可见到什么现象 。
若锥形瓶内盛硝酸银溶液,反应后出现淡黄色,______(填“能”或“不能”)证明苯与溴单质发生取代反应,这是因为___________________________________
(4)反应得到的溴苯呈______色,这是因为 ;为除去混入溴苯中的溴,可加入_____________试剂,用 方法分离。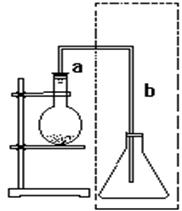

| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. |
反应快慢: Mg>Fe>Cu |
反应物的性质越活泼,反应速率越快. |

 .据报道,最近科学家合成了一种有抗癌活性的化合物Depudecin,其结构简式如下:
.据报道,最近科学家合成了一种有抗癌活性的化合物Depudecin,其结构简式如下:



| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快. |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com