
题目列表(包括答案和解析)
将10.5 g锌、铁、镁粉混合物与一定量的质量分数为25%的稀硫酸恰好完全反应,蒸干溶液后得固体(不含结晶水)29.7g., 则产生氢气的质量为 ( )
A. 1.92g B.0.2g C.0.4g D. 无法求得
在100mL混合溶液中,HNO3和H2SO4物质的量浓度分别为0.4mol/L和0.1mol/L,向该溶液中加入1.92g铜粉,加热,待充分反应后,所得溶液中Cu2+物质的量浓度(mol/L)为 ( )
A.0.15 B.0.20 C.0.225 D.0.45
在100mL混合溶液中,HNO3和H2SO4物质的量浓度分别为0.4mol/L和0.1mol/L,向该溶液中加入1.92g铜粉,加热,待充分反应后,所得溶液中Cu2+物质的量浓度(mol/L)为 ( )
A.0.15 B.0.20 C.0.225 D.0.45
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是
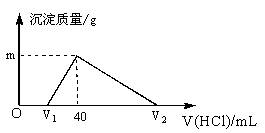
A.原合金质量为0.92g
B.产生氢气的体积为896mL(标准状况下)
C.图中m的值为1.56
D.图中V2为60
将1.92g铜粉与一定量的浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况下),则消耗硝酸的物质的量是
A.0.12mol B.0.09mol C.0.11mol D.0.08mol
题号
1
2
3
4
5
6
7
8
答案
D
C
D
B
D
A
B
C
题号
9
10
11
12
13
14
答案
BD
BC
AD
B
A
D
15.(11分)
(1)1S2 2S2 2P6 3S2 3P5(1分)
(2)6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑(2分)
(3)(共3分)促进氯气从反应混合物中逸出(1分);
稀盐酸(1分);
盐酸还原已生成的碘酸氢钾(1分)。
(4)KOH;KH(IO3)2+KOH=2KIO3+H2O(各1分,共2分)
(5)反应产生的氯气跟KOH反应生成KClO(1分),
KClO能将KIO3氧化成KIO4(1分)从而不能得到碘酸钾(1分)。(共3分)
16.(11分) ( l ) 控制气流速度 让气体混合均匀 干操混合气体.(各1 分)
 (2 ) 吸收过量的氯气(1 分) (3)分液(1 分)
(2 ) 吸收过量的氯气(1 分) (3)分液(1 分)
(4)CH4 + 2Cl
(5)A B(各得1分,选错为0) (6)2.05mol/L(2分)
17.(6分)⑴ NH2OH + 2O2― + H+= NO2― + H2O2 + H2O(2分)
⑵ 5.000×10―3 mol?L―1(2分)
⑶ 2MnO4―+5H2O2+6H+=2Mn2++5O2↑+8H2O(2分)
(或Cr2O72―+3H2O2 + 8H+ =2Cr3+ +3O2↑+7H2O)
18.(10分)(1)NH3 NaAlO2
(2)
(3) CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-(HCO3-也可)
CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-(HCO3-也可)
(4)Al4SiC4+2N2 4AlN+SiC+
4AlN+SiC+
(每空2分,条件不写扣1 分)
19、(10分)(1)CH4(g)+H2O(g) CO(g)+3H2(g);△H=+
CO(g)+3H2(g);△H=+
(2分,条件不写扣1分)
(2)增大氮气和氢气的浓度有利于增大反应速率;减小氨气的浓度,增大氮气和氢气的浓度都有利于平衡向正反应方向移动。(各1分)
(3)1.12×108(2分)
(4) (各2分)
(各2分)
20、(16分)(Ⅰ)(1) (2分)(2)③,⑤ (各1分)
(2分)(2)③,⑤ (各1分)
|