
题目列表(包括答案和解析)
| 滴定 序号 |
待测液体积/mL | NH4Fe(SO4)2标准溶液 滴定管起点读数/mL |
NH4Fe(SO4)2标准溶液 滴定管终点读数/mL |
| 1 | 25.00 | 0.02 | 24.02 |
| 2 | 25.00 | 0.08 | 24.06 |
| 3 | 25.00 | 0.12 | 24.14 |
(08鄞州中学月考)金属钛(Ti)性能优越,被称为继铁、铝制后的“第三金属”。工业上以金红石为原料制取Ti的反应为: aTiO2 + bCl2 + cC ![]() aTiCl4 + cCO ……反应①
aTiCl4 + cCO ……反应①
TiCl4 +2Mg ![]() Ti + 2MgCl2 ……反应②
Ti + 2MgCl2 ……反应②
关于反应①、②的分析不正确的是 ( )
① TiCl4在反应①中是还原产物,在反应②中是氧化剂;② C、Mg在反应中均为还原剂,被还原;③ 在反应①、②中Mg的还原性大于C,C的还原性大于TiCl4;④ a=1,b=c=2;⑤ 每生成19.6 g Ti,反应①、②中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②⑤
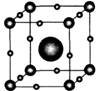
 (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
A.钙钛矿的化学式可表示为![]()
B.钙钛矿晶体中与1个Ca2+距离最近且等距离的O2-有6个
C.太阳能光催化裂解水制氢气的反应可表示为:![]()
D.太阳能光催化裂解水制氢气的反应为放热反应
 (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
A.钙钛矿的化学式可表示为![]()
B.钙钛矿晶体中与1个Ca2+距离最近且等距离的O2-有6个
C.太阳能光催化裂解水制氢气的反应可表示为:![]()
D.太阳能光催化裂解水制氢气的反应为放热反应
(08潍坊模拟)金属钛外观似钢,被誉为“太空金属”。某化学学习小组探讨其性质时发现:钛在室温下与水、稀硫酸、稀盐酸和稀硝酸均不反应,但它能被氢氟酸腐蚀。据此推断,下列表述中正确的是( )
①氢氟酸的酸性比其它酸强
②氢氟酸的氧化性比其它酸强
③氢氟酸的还原性比其它酸强
④钛离子能与氟离子形成难电离和可溶微粒
A.④ B.①② C.③④ D.①②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com