
题目列表(包括答案和解析)
| SO | 2- 4 |
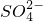 、CuS、Cu2S分别都能在空气中灼烧生成CuO和SO2.
、CuS、Cu2S分别都能在空气中灼烧生成CuO和SO2.| SO | 2-4 |
某实验小组同学在做铜与浓硫酸反应实验时,发现铜片反应结束后,试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有水的烧杯中,发现所得溶液为蓝色,仍然有黑色固体未溶解。
(1)由上述实验可知,原试管底部的白色固体是_____________。
(2)小李同学认为CuO可能不溶于浓硫酸并猜测黑色固体为CuO,小王根据上述实验立即否定了小李的猜测,小王的依据是____________________________________。
(3)为探究黑色固体的组成,小组成员上网检索,获知黑色固体可能是CuS、Cu2S或它们的混合物,同时获知CuS、Cu2S都能被硝酸氧化为Cu2+和SO42-、都能在空气中灼烧生成CuO和SO2。
①写出CuS溶于浓硝酸的化学方程式:_____________________________________。
②将烧杯中黑色固体过滤并洗涤干净,加入少量浓硝酸,待固体溶解后再加入少量BaCl2溶液。该实验过程中,能说明黑色固体中含Cu、S两种元素的实验现象是_________________。
③若你是该实验小组成员,要进一步探究黑色固体到底是CuS、Cu2S还是它们的混合物,应如何设计实验?请简要叙述:___________________________________。
某兴趣小组在实验室用铜和硫酸为原料,采用多种方法制取硫酸铜,制备方法如下:
方法一
⑴甲同学取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到白色沉淀。甲同学为了验证其中白色沉淀的主要成分,设计下列实验。
实验步骤:倾倒掉上层液体后,向所得白色的固体中加入适量蒸馏水,边加边搅拌。
实验现象:白色物质溶解,溶液变为蓝色。
实验结论:所得白色固体的化学式为 。
(2)乙同学与甲同学做相同的实验,还观察到加热过程中,试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失,同时产生能使品红溶液褪色的气体,淡黄色固体消失的原因是(用化学反应方程式回答) 。直到最后反应完毕,发现试管中还有铜片剩余。
方法二
(3)丙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2 2CuO,CuO+H2SO4=CuSO4+H2O。
2CuO,CuO+H2SO4=CuSO4+H2O。
对比甲的方案,你认为丙同学的优点是①_________________________,②_ 。
方法三
⑷丁同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色,写出反应的化学反应方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com