
题目列表(包括答案和解析)
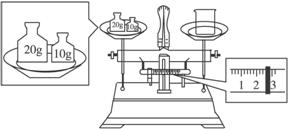
(1)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如下图。由图中可以看出,该同学在操作时的一个错误是____________________,烧杯的实际质量为_______________g。
(2)指出下面实验中各存在的两个错误:
A.需配制150 mL 0.2 mol·L-1NaCl溶液,右图是该同学转移溶液的示意图。

_______________________________________________________________________。
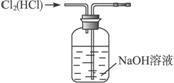
B.除去氯气中的氯化氢气体:
_______________________________________________________________________。
(3)用98%密度为1.84 g·cm-3的浓硫酸配制1 000 mL 0.1 mol·L-1稀硫酸。
①应用量筒量取浓硫酸___________________mL。
②配制硫酸溶液时需要用到的仪器有________________。(除量筒外,写出其余四种)
③下列操作结果,所配溶液物质的量浓度偏低的是________________。
A.没有将洗涤液转移到容量瓶中
B.容量瓶洗净后未经干燥处理
C.定容时仰视观察液面
D.摇匀后立即观察,发现溶液未达刻度线,再用滴管加几滴蒸馏水至刻度线
(每空3分,共12分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g)CH3OH(g)根据题意完成下列各题:
(1)在500℃,从反应开始到刚好达到平衡,氢气的平均反应速率ν(H2)= (用图中相应字母表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的![]() ,下列有关该体系的说法正确的是 (填序号)
,下列有关该体系的说法正确的是 (填序号)
a 氢气的浓度减少 b 正反应速率加快,逆反应速率变慢,平衡正向移动
c 甲醇的物质的量增加 d 重新平衡时c(CO)/c(CH3OH)增大
(3)从反应的方向判断,正向进行的反应 (填序号:A. 高温时 B.低温时 C.任何温度都能 D.任何温度都不能)自发进行。
(4)在不改变反应物用量的情况下,提高CO的转化率采取的措施是
(答两点即可)
(每空3分,共12分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇:CO(g)+2H2(g) CH3OH(g)根据题意完成下列各题:
CH3OH(g)根据题意完成下列各题:
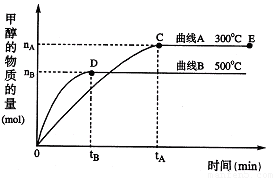
(1)在500℃,从反应开始到刚好达到平衡,氢气的平均反应速率ν(H2)= (用图中相应字母表示)
(2)在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的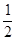 ,下列有关该体系的说法正确的是
(填序号)
,下列有关该体系的说法正确的是
(填序号)
a 氢气的浓度减少 b 正反应速率加快,逆反应速率变慢,平衡正向移动
c 甲醇的物质的量增加 d 重新平衡时c(CO)/c(CH3OH)增大
(3)从反应的方向判断,正向进行的反应 (填序号:A. 高温时 B.低温时 C.任何温度都能 D.任何温度都不能)自发进行。
(4)在不改变反应物用量的情况下,提高CO的转化率采取的措施是
(答两点即可)
(每空3分,共12分) A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。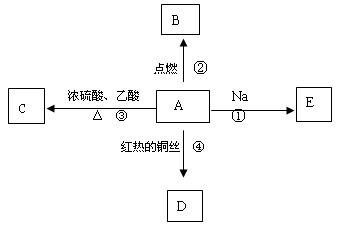
(1)写出A的结构式
(2)写出下列反应的化学方程式(有机物用结构简式表示):
反应①:
反应②:
反应④:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com