
题目列表(包括答案和解析)
| 0.14CV |
| m |
| 14CV |
| m |
| 0.14CV |
| m |
| 14CV |
| m |
| ||
| △ |
 ( )→( )→( )→收集气体
( )→( )→( )→收集气体| 催化剂 |
| 加热 |
| 催化剂 |
| 加热 |
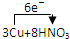 =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2O =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2OI.下列实验操作、试剂保存方法和实验室事故处理,一定正确的是 (填序号)。
A.实验室中,浓硝酸保存在带橡胶塞的棕色细口试剂并中;
B.制备氢氧化铁胶体时,应向20mL沸水中逐滴滴加1~2mL饱和的FeCl3溶液,并继续加热到液体呈透明的红褐色为止;
C.在石油的分馏实验中,温度计需插入液体中;
D.不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液;
E用酸式滴定管量取20.00mL高锰酸钾酸性溶液;
F.在进行中和热测定时,为保证实验的准确性,我们可以采取以下具体措施:使用碎泡沫以起到隔热保温的作用、使用铜质搅拌棒进行搅拌、取用的碱溶液略过量、进行两到三次实验取平均值。
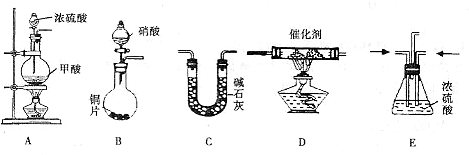
II.汽车尾气的主要成分为CO2及CO、NOX(NO和NO2)的混合物,其中NO的体积分数占95%以上)等。治理方法之一是在汽车排气管上加装“催化转换器”,利用催化剂使CO和NOX发生反应大部分转化为CO2和N2。某小组在实验室利用下图所示装置模拟处理汽车尾气中CO和NOX的反应并测量反应后混合气体的组成。(已知 )
)

试回答下列问题:
(1)仪器的连接顺序为
(2)E装置的作用是___________________、___________________________________________。
(3)写出D中的NOX与CO反应的化学方程式______________________________________。
(4)若B容器中生成的NOX为NO,写出该反应的化学方程式,并标出电子转移的方向和数目_________________________________________________________。
(5)若通入的NOX为NO,C装置增重8.8g,收集到的气体在标准状况下为4.48L(其相对分子质量为28.4)。则收集到的气体中NO的物质的量为___________________。
(6)选择高效催化剂,将汽车尾气转化为无毒气体,便彻底解决了汽车尾气对环境的影响,这种说法是否正确并阐述理由:___________________________________________。
 CO↑+H2O)
CO↑+H2O)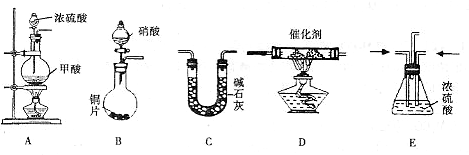
 →→→收集气体
→→→收集气体第Ⅰ卷 (选择题共48分)
一、单项选择题:(本题包括8小题,每题3分,共24分。每小题只有一个选项符合题意)
1、C 2、B 3、B 4、A 5、C 6、A 7、D 8、D
二、不定项选择题(本题包括6小题,每小题4分,共24分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
9、D 10、BC 11、AD 12、A 13、C 14、B
第Ⅱ卷 (选择题共72分)
三、(本题包括1小题,共10分)
15.(10分) 每空2分
I AB
II(1)SiO2 (2)保持较大的C2O42-离子浓度,使Ca2+沉淀完全。
(3)降低CaC2O4在水中的溶解度,减少沉淀的损失,降低实验误差。
(4) 或
或 %
%
四、(本题包括2小题,共18分)
16.(8分)
(1)第三周期第VIIA族 (2分)
(2) 2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ?mol-1 (2分)
2SO3(g) △H=-196.6 kJ?mol-1 (2分)
 (3)Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分) (4) H2O (2分)错误!链接无效。
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分) (4) H2O (2分)错误!链接无效。
17.(10分)
(1) (2分)
(2)8Al+3Fe3O4 4Al2O3+9Fe (2分)
4Al2O3+9Fe (2分)
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
(4)阳极:6O2--12e-=3O2↑;阴极:4Al3++12e-=4Al (每空1分)
(5)③ (2分)
五、(本题包括1小题,共10分)
18.(10分)(每空2分)
 (1) ③⑤
(1) ③⑤
(2)
(3) ①如2Na+2H2O=2Na++2OH-+H2↑;
②如CH3COOH+NH3×H2O=CH3COO-+NH4++H2O;
③如Al3++3H2O Al(OH)3+3H+;
Al(OH)3+3H+;
六、(本题包括1小题,共12分)
19.( 12分)每空2分
12分)每空2分
⑴过滤 低温蒸发结晶
⑵(如图或其他能防止氨气倒吸的装置)
⑶ 冷凝管
⑷ ① 2CaSO4
2CaO+2SO2↑+O2↑
2CaSO4
2CaO+2SO2↑+O2↑
② 95.6%
七、(本题包括1小题,共8分)
20.(8分)
解:(1)6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O (2分)
(2)n(Fe)=×2=0.035 mol
n(SO42-)==0.045 mol
n(OH-)=3×n(Fe3+)-2×n(SO42-)=3×0.035 mol-2×0.045 mol=0.015 mol (2分)
盐基度=×100%= ×100%=14.29% (2分)
(3)n(H2O)=
=0.054 mol
化学式: Fe35(OH)15(SO4)45?54H2O (2分)
八、(本题包括1小题,共14分)
21.(14分)
(1)相同 b (每空1分)
(2)B(2分)
(3)I.3d24S2 (2分) II.[TiCl(H2O)5]Cl2?H2O(2分)
(4)I.KO2 kJ?mol-1 (每空2分,共
射阳中学2009届高三上学期第二次月考
化 学 答 题 纸
三、(本题包括1小题,共10分)
15.(10分)
I
II(1)
(2)
(3)
(4)
四、(本题包括2小题,共18分)
16.(8分)
(1)
(2)
(3)
(4)
17.(10分)
(1)
(2)
(3)
(4)阳极 阴极
五、(本题包括1小题,共10分)
18.(10分)
(1)
(2) 
(3) 请在下列表格中用相应的“离子方程式”否定这些观点。
①所有的离子方程式均可以表示一类反应
②酸碱中和反应均可表示为:H++OH-=H2O
③离子方程式中凡是难溶性酸碱盐(产物)均要用“↓”
六、(本题包括1小题,共12分)
19.(12分)
(1)
(2) 
(3)
(4)①
②
七、(本题包括1小题,共8分)
20.(8分)
(1)
(2)
(3)
八、(本题包括1小题,共14分)
21.(14分)
(1)
(2)
(3)I II
(4) I II
 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com