
题目列表(包括答案和解析)
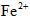 34%~36%,是糖衣片,……,与
34%~36%,是糖衣片,……,与 (维生素C)同服可增加本品吸收。某同学设计实验时对其中的铁成分进行了验证。请完成该实验:
(维生素C)同服可增加本品吸收。某同学设计实验时对其中的铁成分进行了验证。请完成该实验: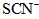 生成
生成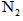 、
、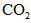 和SO42-,也可以将
和SO42-,也可以将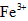 氧化成
氧化成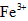 。
。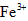 离子存在。该离子存在的原因可能是(填序号):___________________
离子存在。该离子存在的原因可能是(填序号):___________________ 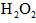 溶液,溶液的红色先变深,之后红色逐渐褪去。
溶液,溶液的红色先变深,之后红色逐渐褪去。  片,片刻后溶液红色也褪去,说明
片,片刻后溶液红色也褪去,说明 有___________性。
有___________性。
(14分)亚铁是血红蛋白的重要组成部分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,与VC(维生素C)同服可增加本品吸收。某同学设计实验对其中的铁成分进行了验证。请一起完成实验:
第一步:查阅资料得知,双氧水可以氧化SCN—生成N2、CO2、和SO42—,也可以将Fe2+ 氧化成 Fe3+。
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色混浊液,说明有 存在(填离子符号)。
第三步:往上述溶液中滴入几滴KSCN溶液出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是(填序号):
①药品中的铁本来就以Fe3+的形式存在:②在制药过程中生成少量Fe3+;
②本实验过程中有少量Fe3+生成。
第四步:将第三步所得溶液分成两份,分别装在A、B两个试管中。
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。
红色变深的原因是(用离子方程式表示) 红色又逐渐褪去的原因可能是
设计实验证明你的推测
第六步:向B试管的溶液中加入一片VC,片刻后溶液红色也褪去,说明VC有 性。怎样理解药品说明书中所述“与VC(维生素C)同服可增加本品吸收”这句话?
。
(14分)亚铁是血红蛋白的重要组成部分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,与VC(维生素C)同服可增加本品吸收。某同学设计实验对其中的铁成分进行了验证。请一起完成实验:
第一步:查阅资料得知,双氧水可以氧化SCN—生成N2、CO2、和SO42—,也可以将Fe2+ 氧化成 Fe3+。
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色混浊液,说明有 存在(填离子符号)。
第三步:往上述溶液中滴入几滴KSCN溶液出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是(填序号):
①药品中的铁本来就以Fe3+的形式存在:②在制药过程中生成少量Fe3+;
②本实验过程中有少量Fe3+生成。
第四步:将第三步所得溶液分成两份,分别装在A、B两个试管中。
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。
红色变深的原因是(用离子方程式表示) 红色又逐渐褪去的原因可能是
设计实验证明你的推测
第六步:向B试管的溶液中加入一片VC,片刻后溶液红色也褪去,说明VC有 性。怎样理解药品说明书中所述“与VC(维生素C)同服可增加本品吸收”这句话?
。
(14分)亚铁是血红蛋白的重要组成部分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,与VC(维生素C)同服可增加本品吸收。某同学设计实验对其中的铁成分进行了验证。请一起完成实验:
第一步:查阅资料得知,双氧水可以氧化SCN—生成N2、CO2、和SO42—,也可以将Fe2+氧化成 Fe3+。
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色混浊液,说明有 存在(填离子符号)。
第三步:往上述溶液中滴入几滴KSCN溶液出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是(填序号):
①药品中的铁本来就以Fe3+的形式存在:②在制药过程中生成少量Fe3+;
②本实验过程中有少量Fe3+生成。
第四步:将第三步所得溶液分成两份,分别装在A、B两个试管中。
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。
红色变深的原因是(用离子方程式表示) 红色又逐渐褪去的原因可能是
设计实验证明你的推测
第六步:向B试管的溶液中加入一片VC,片刻后溶液红色也褪去,说明VC有 性。怎样理解药品说明书中所述“与VC(维生素C)同服可增加本品吸收”这句话?
。
第Ⅰ卷(选择题 共48分)
题号
1
2
3
4
5
6
7
8
答案
A
C
C
C
B
B
A
D
题号
9
10
11
12
13
14
答案
AB
D
C
B
BD
CD
第Ⅱ卷(非选择题部分 共72分)
15.(10分)(1)①B(1分) ②蒸馏烧瓶(1分) ③气密性检查(2分)
④大气压(或开始时烧瓶内的压强)(1分) 强(1分)
开始一段时间内曲线a的变化值大于曲线b。(2分)
(2)①有利于控制氧气的量 ②有利于二氧化锰的回收
③有利于控制氧气的生成速率(答出任意两点即可,每空1分)
16.(12分)(1)② 2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- (2分)
 |
⑤ NH4++HCO3-+2OH- CO32-+NH3↑+2H2O(2分)
(2)过滤(1分) 加热(1分) (3)碱石灰(或硅胶)(1分)
(4)AlN(2分) 配位键(1分)
(5)产生等量的NH3时,(NH4)2CO3所消耗的NaOH的量是NH4HCO3一半。(2分)
17.(10分)⑴ 0.125 4.69 ⑵增大 > ⑶0.25 不变 (以上每空1分)
(4)6 1.25 (每空2分)
18.(10分)(1)②⑥(2分)
(2)C: (1分) F:
(1分) F:
 (1分)
(1分)
(3)
|