
题目列表(包括答案和解析)
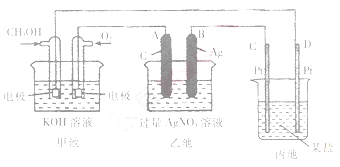
(11分)下图是一个化学过程的示意图。
(1)请回答图中甲池是______装置,其中OH-移向________极(填“CH3OH”或“O2”)
(2)写出通入CH3OH的电极的电极反应式_________。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为_________极(填“A”或“B”),并写出此电极反应的电极反应式____________。
(4)乙池中反应的离子方程式为____________。
(5)当乙池中B(Ag)极的质量增加5.40g时,乙池的pH是________(若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是_______(填序号).
| A.MgSO4 | B.CuSO4 | C.NaCl | D.AgNO3 |
| A.MgSO4 | B.CuSO4 | C.NaCl | D.AgNO3 |
(1)写出三种元素的名称:X________,Y________,Z________。
(2)两种氧化物分别为________和________。
(3)Z的单质溶于水,滴加到X和Y形成的化合物的水溶液中,其离子方程式为(要求标明电子转移方向和总数)________________。
(4)用电子式表示Y的质量分数为74.19%的氧化物的形成过程________________。
已知X的阴离子核外电子排布与氙的原子核外电子排布相同;Y有两种氧化物,其水溶液都呈碱性。在Y的两种氧化物中,Y的质量分数分别是74.19%和58.97%,这两种氧化物的摩尔质量分别是62g×mol-1和78g×mol-1。在X和Y化合的生成物的水溶液中滴入Z单质的水溶液,溶液由无色变为深黄色。Z和X在同一主族,相差2个周期。试回答:
(1)写出三种元素的名称:X________,Y________,Z________。
(2)两种氧化物分别为________和________。
(3)Z的单质溶于水,滴加到X和Y形成的化合物的水溶液中,其离子方程式为(要求标明电子转移方向和总数)________________。
(4)用电子式表示Y的质量分数为74.19%的氧化物的形成过程________________。
(11分)(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还生成硝酸钠和氯化钠等。
①写出制取高铁酸钠的化学方程式: ;
②在制取高铁酸钠的反应中 元素被氧化;
③高铁酸钠之所以有净水作用,除杀菌外,另一个原因是 。
(2)在某化工厂生产中,要用到一种无色、可溶于水的晶体铝铵矾。该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵。向该复盐的浓溶液中逐滴加入浓氢氧化钠溶液。将发生一系列变化。已知,NH4+与AlO2—在水溶液中不能大量共存,会发生如下反应:NH4++A1O2—+H2O=Al(OH)3↓+NH3↑
试回答:
①硫酸铝铵在水溶液中的电离方程式为 ;
②在逐滴加入浓氢氧化钠溶液的过程中,产生的现象有:a溶液中出现白色沉淀;b有刺激性气体逸出;c白色沉淀量逐渐增多;d白色沉淀完全消失;e白色沉淀逐渐减少。
请回答各种现象由先到后出现的顺序是(用序号回答): 。
③并在下图中画出氢氧化钠的加入体积与沉淀量的关系.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com