
题目列表(包括答案和解析)
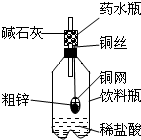 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ||
| ②将铜网插入足量稀盐酸中,充分反应 | 发生的化学方程式: | |
| ③反应完全后,称得装置总质量为119.8g | 产生H2的质量为 粗锌的纯度为 |
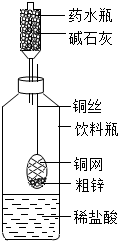 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告. 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告.| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ∕ | ∕ |
| ②将铜网插入足量稀盐酸中,充分反应 | 粗锌表面产生气泡 粗锌表面产生气泡 |
发生的化学方程式: Zn+2HCl═ZnCl2+H2↑ Zn+2HCl═ZnCl2+H2↑ |
| ③反应完全后,称得装置总质量为119.8g | ∕ | 产生H2的质量为 0.2 0.2 g.粗锌的纯度为 65% 65% . |
 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请帮助完成下列实验报告| 实验内容和步骤 | 实验现象 | 结论(或化学方程式) |
| ①称量10.0g粗锌放在铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g | ||
| ②将铜网插入足量稀盐酸中,充分反应 | 发生的化学方程式: | |
| ③反应完全后,称得装置总质量为119.8g | 产生H2的质量为______g. 粗锌的纯度为______ |
 某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告.
某同学利用日常生活中常见的用品制作了一套如图装置,用该装置对粗锌样品进行实验.请你帮助完成下列实验报告.一、选择题
题号
1
2
3
4
5
6
7
8
9
10
11
答案
B
A
B
C
A
D
C
A
D
B
C
题号
12
13
14
15
16
17
18
19
20
21
22
答案
D
C
A
A
B
D
C
D
C
B
D
二、填空题
23.(1)2Cu2+ (2)3NO2
24.A ;B
25.(1)267(2)4;41
26.H2;O2;C;CO;Ca(OH)2;
27.(1)CO2(2)NaOH(3)CH4(4)SO2
28.(1)K2SO4+Ba(NO3)2==BaSO4↓+2KNO3 ,复分解反应
(2)CaCO3+2HCl==CaCl2+CO2↑+H2O Mg(OH)2+2HCl==MgCl2+2H2O
CaCO3+2HAc==Ca(Ac)2+CO2↑+H2O
(3)CaH2+2H2O ==Ca(OH)2 +2H2 ↑ Ca(OH)2 +Na2CO3== CaCO3↓+2NaOH
或CaH2+2H2O+Na2CO3== CaCO3↓+2NaOH+2H2 ↑
三、推断题
29.(1)FeCl3 (2)Fe(NO3)3、NaCl、NaNO3,HCl、HNO3
30.(1)HCl(2)H2(3)第一种情况:H2、N2、HCl; 第二种情况:H2、N2、HCl、CO;
第三种情况:H2、N2、HCl、CO2; 第四种情况:H2、N2、HCl、CO、、CO2
四、实验题
31.(1)① 试管 ② 烧杯(2)BD;CFG;AE;
32.(一)测定粗锌的纯度(含量、质量分数等)
(三)现象:粗锌表面产生气泡
方程式:Zn+2HCl==ZnCl2+H2↑H2质量:0.2;纯度:65%
(四)(1)吸收氢气中的HCl和H2O;偏大(2)不能。
理由:产生的CO2 将被碱石灰吸收,得不到生成的CO2质量。(4)偏小
五、计算题
33.(1)解:设原固体中Na2CO3的质量为x,消耗盐酸的质量为y
Na2CO3 + 2HCl= 2NaCl+CO2↑+H2O
106 73 44
x 7.3%y 8.8g 106:x = 73:7.3%y = 44:8.8g
∴x = 21.2g y=200g
∴原固体中Na2CO3 的质量分数=
消耗盐酸溶液的质量为200g。
(2) 第一次逐滴加盐酸100g:0
CO2 质 量 /g 8.8 0
100 200 300 稀盐酸质量/g 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。
ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号