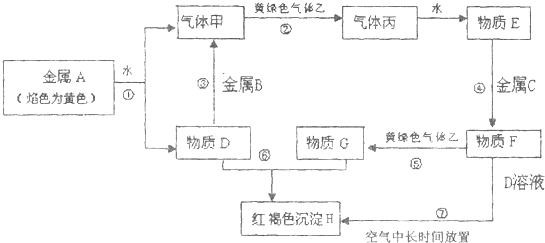
立足教材实验是掌握高中化学实验的基础,是理解化学科学的实验原理、实验方法和实验思路,提高学生实验能力的基本途径.
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮.观察钠的颜色.这个实验中还需用到的一种仪器是
镊子
镊子
;
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯.把反应的现象和相应结论填入空格.“浮”---钠的密度比水小;
“熔”---
钠的熔点低,反应放热
钠的熔点低,反应放热
;
“红”---反应生成了氢氧化钠;
(3)实验3:在两支试管里分别加入5mL 盐酸和5mL NaOH溶液,在各放入一小段铝片,观察实验现象.试写出铝和NaOH溶液反应的离子方程式:
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
;
(4)实验4:把水滴入盛有Na
2O
2固体的试管中,立即用带火星的木条放在试管口,检验生成的气体.向反应后的溶液中加入酚酞试液,可以看到
溶液先变红后褪色
溶液先变红后褪色
;
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气.该氧化还原反应的氧化剂是
水蒸气
水蒸气
;
(6)实验6:在试管里注入少量新制备的FeSO
4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色.发生这种颜色变化的原因是(用化学方程式表示):
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.

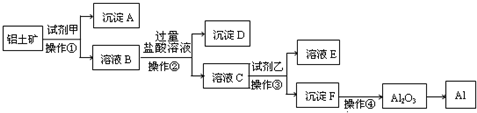

 ]2-Na+
]2-Na+ ]2-Na+
]2-Na+