
题目列表(包括答案和解析)
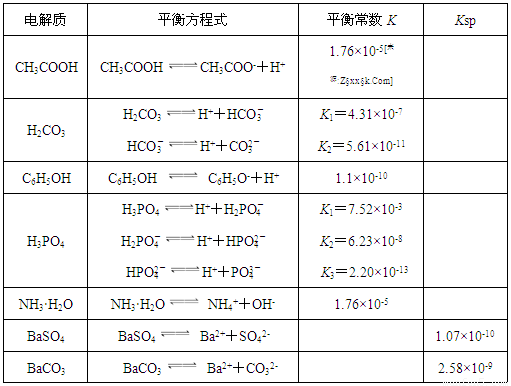
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp (25℃)。
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为 (须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式: ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml0.01mol/L氨水,混合溶液中粒子浓度关系正确的是 ;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c((NH4+)>c (C6H5O-) >c(H+)>c (OH-)
C.V=10时,混合液中水的电离程度小于10ml0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+2 c (NH4+)= c (C6H5O-)+c (C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式 。
(6)Ⅰ.如下图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
① T1 T2(填>、=、<),
T2温度时Ksp(BaSO4)= ;
② 讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次。[提示: BaSO4(s)+ CO32- (aq) BaCO3(s)+ SO42- (aq) ]
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp (25℃)。
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为 (须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式: ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是 ;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c((NH4+) >c (C6H5O-) >c (H+)>c (OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+ 2 c (NH4+)= c (C6H5O-)+ c (C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式 。
(6)Ⅰ.如下图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
① T1 T2(填>、=、<),
T2温度时Ksp(BaSO4)= ;
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为 1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次。[提示: BaSO4(s)+ CO32- (aq)
1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次。[提示: BaSO4(s)+ CO32- (aq) BaCO3(s)+ SO42- (aq) ]
BaCO3(s)+ SO42- (aq) ]
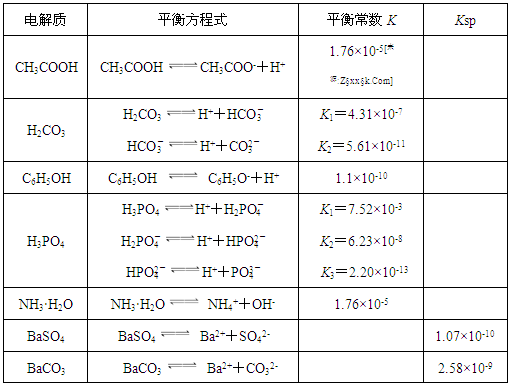
下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp (25℃)。
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为 (须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式: ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是 ;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c((NH4+) >c (C6H5O-) >c (H+)>c (OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+ 2 c (NH4+)= c (C6H5O-)+ c (C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式 。
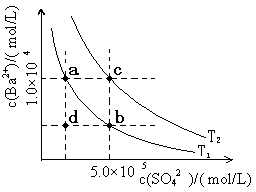
(6)Ⅰ.如下图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
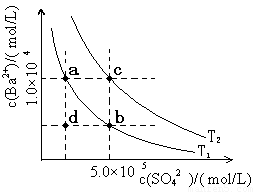
① T1 T2(填>、=、<),
T2温度时Ksp(BaSO4)= ;
② 讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次。[提示: BaSO4(s)+ CO32- (aq) BaCO3(s)+ SO42- (aq) ]
BaCO3(s)+ SO42- (aq) ]
 1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次。[提示: BaSO4(s)+ CO32- (aq)
1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理 次。[提示: BaSO4(s)+ CO32- (aq) BaCO3(s)+ SO42- (aq) ]
BaCO3(s)+ SO42- (aq) ]在二氧化碳的水溶液中存在着如下平衡:
C02(g)  C02(aq)
C02(aq)+H20
C02(aq)
C02(aq)+H20 H2C03(aq)
H2C03(aq)
H2C03(aq)  H+ (aq)+HCO3-(aq)
HCO3-(aq)
H+ (aq)+HCO3-(aq)
HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
下列有关说法正确的是( )
A.水中溶解的二氧化碳的浓度,夏天时比冬天时高
B.如果海水略呈碱性,海水中二氧化碳的浓度比纯水高
C.气压升高,水中c(HCO3-)增大
D.常温下,二氧化碳的水溶液中,由水电离出的c(H+)与c(OH-)的乘积等于1×lO-14
一、选择题
1.C 2.B 3.D 4.B 5.A 6.C 7.D 8.C
9.C 10.A 11.B 12.D l3.D 14.C 15.C
二、选择题
16. B 17. BD 18.C 19. A 20. AD 21. BC 22.C
23.(1)500Ω(2分)2.00(2分)
(2) mㄑM(1分) (2) ACD(2分)(3)C:平衡摩擦力时,长木板的倾角过大
了; D:没有平衡摩擦力或木板的倾角过小。(4分)
24.(16分)
解:
(1)设粒子从电场中飞出时的侧向位移为h, 穿过界面PS时偏离中心线OR的距离为y
则: h=at2/2 (1分)
又 
 即:
即: (2分)
(2分)
代入数据,解得: h=0.03m=3cm (1分)
带电粒子在离开电场后将做匀速直线运动,由相似三角形知识得:
 (2分)代入数据,解得: y=0.12m=12cm
(2分)
(2分)代入数据,解得: y=0.12m=12cm
(2分)
(2)设粒子从电场中飞出时沿电场方向的速度为vy,则:vy=at= 
代入数据,解得: vy=1.5×106m/s (1分)
所以粒子从电场中飞出时的速度大小为:
 (1分)
(1分)
设粒子从电场中飞出时的速度方向与水平方向的夹角为θ,则:

 (2分)
(2分)
因为粒子穿过界面PS最后垂直打在放置于中心线上的荧光屏上,所以该带电粒子在穿
过界面PS后将绕点电荷Q作匀速圆周运动,其半径与速度方向垂直。
匀速圆周运动的半径:  (1分)
(1分)
由:  (2分)代入数据,解得: Q=1.04×10-8C (1分)
(2分)代入数据,解得: Q=1.04×10-8C (1分)
(说明:其它方法正确按步骤参照给分)
25.(18分)
(1)金属棒下滑1 m过程中,流过棒的电量可以用
 (4分)
(4分)
(2)由于棒从静止开始运动,因此首先可以确定棒开始阶段
 做加速运动,然后通过受力分析,看看加速度可能如何变化?
做加速运动,然后通过受力分析,看看加速度可能如何变化?
如图所示,棒在下滑过程中沿导轨方向有向下的重力分力
 和向上的安培力F。由于m随位移
和向上的安培力F。由于m随位移 增大而增大,所
增大而增大,所
以, 是一个变力;而安培力与速度有关,也随位移增
是一个变力;而安培力与速度有关,也随位移增
大而增大,如果两个力的差值恒定,即合外力是恒力的话,棒
有可能做匀加速运动。 (2分)
假设棒做的是匀加速运动,且设下滑位移 时的加速度为
时的加速度为 ,根据牛顿第二定律,有
,根据牛顿第二定律,有
 (1分)
(1分)
而安培力 (1分)
(1分)
所以
假设棒做匀加速直线运动,则瞬时速度 ,由于
,由于 ,代入后得:
,代入后得:

 ① (2分)
① (2分)
从上述方程可以看出 的解是一个定值,与位移
的解是一个定值,与位移 无关,这表明前面的假设成立,棒的
无关,这表明前面的假设成立,棒的
运动确实是匀加速直线运动。若 与位移
与位移 有关,则说明
有关,则说明 是一个变量,即前面的假
是一个变量,即前面的假
设不成立。 (2分)
(3)为了求棒下滑2 m时的速度,应先求出棒的加速度。将题目给出的数据代①式得到


令 则
则
解得 ,
, (舍去)即加速度
(舍去)即加速度 (2分)
(2分)
根据匀变速运动规律,
此时电阻R上的电流 (4分)
(4分)
26.(1)下丘脑 大脑皮层 (2)C→D→F A-→ B (3)胰高血糖素 肾上腺素
(4)幼年期甲状腺激素分泌不足会影响大脑的生长发育
27.(1)清水 逐渐变小
(2)在盖玻片一侧滴入质量浓度为0.1 g/mL的KNO3溶液,另一侧用吸水纸吸引,这样重复几次,使洋葱表皮浸入到KNO3溶液中。用显微镜观察质壁分离发生,一段时间后会自动复原。(4分)K+和NO3-会通过主动运输进入细胞内,使细胞液浓度逐渐升高后,外[JP3]界的水会自动进入细胞内,质壁分离会自动复原。(3)0.5 g/mL的蔗糖溶液
28.(15分)
【探究一】2AI+2NaOH+2H20=2NaAl02+3H2 (2分)
(1)97 (2分) (2)偏高 (1分)
【探究二】(1)不需要 (1分)
(2)检查装置的气密性;合金完全溶解(或加入足量盐酸,或调整量气管C的高度,使C中液面与B液面相平等合理答案)(各1分,共2分)
【探究三】(1)灼烧后固体的质量 (2分) (2)是 (2分)
【实验拓展】铝镁合金 溶液
溶液 测定固体质量
测定固体质量
(或铝镁合金)  溶液
溶液 测定固体质量等合理答案) (3分)
测定固体质量等合理答案) (3分)
29.(13分)
(1)HCHO(或结构简式、甲醛) (1分)
作消毒剂(或作防腐剂、作化工原料等合理答案) (1分) 糖类(或油脂) (1分)
(2)H:N:H (1分)
H
N2+3H2 2NH, (2分) C (2分)
2NH, (2分) C (2分)
(3)NH4++H2OㄐNH3?H2O+H+(或其它合理答案) (2分)
(4)NH4++HCO3-+2OH- = NH3?H2O+H2O+CO32一 (2分)
O

 H2N---CH2一C--OH (1分)
H2N---CH2一C--OH (1分)
30.(14分)
(1)2C2H2+502 = 4C02+2H20 (3分) H2 (2分)
(2)品红溶液 (1分) 品红溶液褪色,加热后,溶液又变成红色 (2分)。
(3)接触室 (1分)。
4FeS2(s)+11O2(g)一2Fe2O3(s)+8SO2(g);△H=-3412kJ?mol一1
(或其它合理答案) (3分) 15/8 (2分)
 【选做部分】
【选做部分】
31.(8分)(1)①CaCO3 CaO+CO2↑(2分)

②MgCl2(熔融) Mg+Cl2↑(2分)
(2)阴极: Mg2++2e-=Mg(2分)
(3)阳极产生的氧气与阳极材料中的碳发生反应而不断地被消耗。(2分)
32.(8分)(1)1s22s22p63s23p2
|