
题目列表(包括答案和解析)
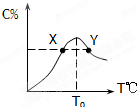 将物质的量均为3.00mol物质A、B混合于5L溶 器中,发生如下反应 3A+B?2C,在反应过程中C的物质的量分数随温度变化如图所示:
将物质的量均为3.00mol物质A、B混合于5L溶 器中,发生如下反应 3A+B?2C,在反应过程中C的物质的量分数随温度变化如图所示:物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50
mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50
mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0325 mol·L-1·min-1
B.保持其他条件不变,若此时再向溶液中加入0.50 mol (t-BuNO)2,重新达平衡时(t-BuNO)2的百分含量减小
C.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率小于65%
D.保持其他条件不变,升高温度, (t-BuNO)2的平衡转化率大于65%,则其能量关系可用下图表示


 B(s)+D(g) △H=akJ/mol(a>0),该温度下平衡常数K=0.263。若生成1 mol B,则吸收的热量____(选填“大于”、“等于”或“小于”)a kJ;若加入过量的A,则C的转化率__ (选填“升高”、“不变”或“降低”);若容器内压强不再随时间变化,则该反应__ (选填“达到”、“未达到”或“不一定达到”)化学平衡状态;该反应达到化学平衡状态时,若c( C) =0. 100 mol/L,则c(D)=___mol/L。
B(s)+D(g) △H=akJ/mol(a>0),该温度下平衡常数K=0.263。若生成1 mol B,则吸收的热量____(选填“大于”、“等于”或“小于”)a kJ;若加入过量的A,则C的转化率__ (选填“升高”、“不变”或“降低”);若容器内压强不再随时间变化,则该反应__ (选填“达到”、“未达到”或“不一定达到”)化学平衡状态;该反应达到化学平衡状态时,若c( C) =0. 100 mol/L,则c(D)=___mol/L。  2(t-BuNO).
2(t-BuNO).


1
2
3
4
5
6
7
8
A
B
C
D
B
C
D
A
9
10
11
12
13
14
15
16
D
A
C
C
A
D
B
B
17.(1)促进, B (2)甲大 (各1分)
乙用氯化铵溶液稀释后,.files/image325.gif) 增大很多,使
增大很多,使.files/image212.gif) 的电离平衡向抑制电离的方向移动;
的电离平衡向抑制电离的方向移动;.files/image328.gif) 发生水解,使稀释后的乙溶液的
发生水解,使稀释后的乙溶液的.files/image330.gif) )增大 (答
)增大 (答.files/image328.gif) 水解使溶液
水解使溶液.files/image153.gif) 减小不给分) (2分)
减小不给分) (2分)
(3)③ 适量的.files/image036.gif) (各1分)
(各1分)
18.(1).files/image335.gif) ,
,.files/image337.gif) ;(各2分)
;(各2分)
(2)①.files/image261.gif) (1分) ②
(1分) ②.files/image340.gif) (1分)
(1分)
得.files/image342.gif)
.files/image343.gif) |
.files/image344.gif)
.files/image345.gif) ③
③.files/image347.gif) (2分)
(2分)
得.files/image349.gif)
④ 1:2 (2分)
19.(1) .files/image351.gif) (各2分)
(各2分)
(2) .files/image353.gif)
(3)0.5 1 (4) D
20.(1)第三周期.files/image355.gif) 族(2分)
族(2分)
(2) .files/image030.gif) 属于分子晶体而
属于分子晶体而.files/image358.gif) 属于原子晶体(2分)
属于原子晶体(2分)
(3) .files/image360.gif) (2分)
(2分)
(4).files/image362.gif) 、
、.files/image364.gif) 、
、.files/image366.gif) 、
、.files/image368.gif) (写出3种即可)(3分)
(写出3种即可)(3分)
21.(1) ③⑤⑦ (2) C (各2分)
22.(1).files/image076.gif) 、
、.files/image030.gif) 等(2分)
等(2分)
(2).files/image372.gif) ;
;.files/image374.gif) ;
;.files/image012.gif) (各1分)
(各1分)
(3)① .files/image377.gif) (1分)
(1分)
②a、b (各1分) .files/image379.gif) (1分) 双手紧握 (或微热) 试管丁使试管中气体逸出,
(1分) 双手紧握 (或微热) 试管丁使试管中气体逸出,.files/image034.gif) 与水接触后即可引发烧杯中的水倒流入试管丁(2分)
与水接触后即可引发烧杯中的水倒流入试管丁(2分)
③
.files/image382.gif) (2分)
(2分)
23.(1).files/image186.gif) (2)
(2).files/image385.gif) (3)
(3).files/image387.gif) (4)
(4) .files/image389.gif) (各2分)
(各2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com