
题目列表(包括答案和解析)
某体积可变的密闭容器,盛有体积比为2:3的N2和H2,在一定条件下发生反应N2(g)+3H2(g)![]() 2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V,其中NH3的体积占20%,下列说法正确的是( )
2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V,其中NH3的体积占20%,下列说法正确的是( )
A.原混合气体的体积为1.2V B.原混合气体的体积为1.1V
C.反应中消耗N2的体积为0.3V D.达到平衡时,消耗H2体积为0.3V
已知:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
(1)450℃时,往一个2L的密闭容器中充入2. 6mol H2和1mol N2, 反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L—1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
| | N2 | H2 | NH3 |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
 4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“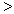 ”、 “
”、 “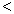 ”或“=”), △H=_____________。
”或“=”), △H=_____________。| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol?L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
| N2 | H2 | NH3 | |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L—1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
| | N2 | H2 | NH3 |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
 4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“ ”、 “
”、 “ ”或“=”), △H=_____________。
”或“=”), △H=_____________。已知:N2(g)+3H2(g)![]() 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
(1)450℃时,往一个2L的密闭容器中充入2. 6mol H2和1mol N2, 反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L—1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
①5 min内,消耗N2的平均反应速率为_______________,此条件下该反应的化学平衡常数K=_______________;反应达到平衡后,若往平衡体系中加入H2、N2和NH3各2mol,此时该反应的v(N2)正_______________v(N2)逆(填写“>”、“=”或“<”=)。
②下列各项能作为判断该反应达到化学平衡状态的依据是__________(填序号字母)
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v(N2)正=3v(H2)逆 C.容器内压强保持不变
D.混合气体的密度保持不变 E.容器内混合气体的平均分子量不变
③若改变某一条件,达新平衡时n(H2)=1.60mol ,下列说法正确的是_____________。
A.平衡一定正向移动 B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度 D.可能是缩小了容器的体积
(2)450℃时,在另一密闭容器中进行上述合成氨的反应,各物质的起始浓度和平衡浓度如下表所示:
| N2 | H2 | NH3 | |
| 起始浓度(mol/L) | 0.2 | 0.3 | 0.2 |
| 平衡浓度(mol/L) | a | b | c |
请回答:
①各物质的平衡浓度可能是_______________.
A.c=0.5mol/L B.b=0.5mol/L C.c=0.4mol/L D.a=0.3mol/L
②a的取值范围是:_______________.
③请用数学表达式表示下列量之间的关系:
(I)a与b的关系:_______________。
(Ⅱ)a、b、c的关系:_______________。
(3) 根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水可发生下列反应:2N2(g)+6H2O(l) ![]() 4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“![]() ”、 “
”、 “![]() ”或“=”), △H=_____________。
”或“=”), △H=_____________。
(已知:H2的燃烧热为285.8 kJ/mol)
选择题答案:
l
2
3
4
5
6
7
8
9
10
D
C
C
C
A
A
B
B
B
B
11
12
13
14
15
16
17
18
19
20
C D
B D
C
B
A
A
A D
C D
B D
B
三、共23分
21.每个空1分:化学能 电能 不会污染环境 0
22.每个空2分:3X+Y.files/image010.jpg) 2Z (不写可逆号扣1分)
2Z (不写可逆号扣1分)
0.05mol?L.files/image035.gif) ?min
?min.files/image035.gif) (不写单位或写错单位不得分)
(不写单位或写错单位不得分)
23.
.files/image038.jpg)
每个空1分(电荷不守恒的扣2分)
电极名称
电极反应式
电极反应类型
正极
2Cu2++4e.files/image006.gif) =2Cu
=2Cu
还原反应
负极
2Zn-4e.files/image006.gif) =2Zn2+
=2Zn2+
氧化反应
阳极
4OH.files/image006.gif) -4e
-4e.files/image006.gif) =O2↑+2H2O
=O2↑+2H2O
氧化反应
阴极
4H++4e.files/image006.gif) =2H2↑
=2H2↑
还原反应
24.每个空1分:
(1)强酸性(不注明“强”的不得分) 2H++2e.files/image006.gif) =H2↑ Fe-2e
=H2↑ Fe-2e.files/image006.gif) =Fe2+
=Fe2+
(2)中性或弱酸性(答不全不得分) O2+4e.files/image006.gif) +2H2O==4OH
+2H2O==4OH.files/image006.gif) 2Fe-4e
2Fe-4e.files/image006.gif) ==2Fe2+
==2Fe2+
(两个电极反应式的电荷不守恒不得分)
四、共18分
25.(1)每个空1分:铁(Fe) 石墨(其它答案不得分)
Fe-2e.files/image006.gif) +2OH
+2OH.files/image006.gif) =Fe(OH)2↓ 2H++2e
=Fe(OH)2↓ 2H++2e.files/image006.gif) =H2↑
=H2↑
(2)B C (选对一个得1分,选对2个得2分,选错一个得0分)
(3)每个空1分:隔绝空气,防止生成的氢氧亚化铁被氧化 加热煮沸 排出溶液中的空气(氧气)
(4)B C (选对一个得1分,选对2个得2分,选错一个得0分)
26..files/image042.gif)
(表中每个空1分)
m
a
y
1
0.25
16.67%
2
0.45
21.43%
3
0.56
19.35%
2:1 (1分)
由表中的数据可知,开始m增大时,y也随之增大;当m>2时,m增大时,y又随之减小,m=2时,y为最大值 (2分)
五、共9分
27.(3分)2:3:1
28.解:△S(298K)=169.6J/(mol?K)=0.1696KJ/(mol?K)…………(1分)
△G=AH(298K)-T?△S(298K)…………………………………(1分)
=178.3KJ/mol-T×0.1696KJ/(mol?K)<0……………(1分)
故:T>178.3KJ/mol÷0.1696KJ/(mol?K)=1051.3K…………(1分)
所以碳酸钙分解的最低温度为1051.3K……………………………(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com