
题目列表(包括答案和解析)
(共12分)光合作用是绿色植物和其他自养型生物利用光能由简单化合物合成高能复杂分子的过程。光合作用中叶绿素分子与特殊的酶分子受体(MS)相结合,发生一系列氧化还原反应。科学家们发现光合作用还存在许多变化形式,如有些细菌可用H2S代替H2O进行光合作用生成结构与性质完全相似的产物。
我国科学家早在1946年就发现铀吸收中子后可发生核裂变分裂成较小的碎片。如以一个慢中子轰击![]() 发生核裂变时,能产生两种核素72X、
发生核裂变时,能产生两种核素72X、![]() 和若干快中子。快中子再与核素72X反应可生成
和若干快中子。快中子再与核素72X反应可生成![]() ,继而生成以上MS中金属M的一种核素。M是应用最广泛的金属之一,在高温高压下与CO作用生成淡黄色液体A(A在高温下可分解为M和CO)。含有M的一种深红色化合物晶体B具有顺磁性,在碱性溶液中B能把Cr(Ⅲ)氧化为CrO42-,而本身被还原成C。溶液中C可被氯气氧化成B。固体C在高温下可分解,其产物为碳化物D,剧毒的钾盐E和化学惰性气体F。A继续与CO作用可形成满足18电子规则的金属有机化合物M2(CO)9。(18电子规则指过渡金属有机化合物中,金属的价电子和配体提供或共享的电子总数等于18)。
,继而生成以上MS中金属M的一种核素。M是应用最广泛的金属之一,在高温高压下与CO作用生成淡黄色液体A(A在高温下可分解为M和CO)。含有M的一种深红色化合物晶体B具有顺磁性,在碱性溶液中B能把Cr(Ⅲ)氧化为CrO42-,而本身被还原成C。溶液中C可被氯气氧化成B。固体C在高温下可分解,其产物为碳化物D,剧毒的钾盐E和化学惰性气体F。A继续与CO作用可形成满足18电子规则的金属有机化合物M2(CO)9。(18电子规则指过渡金属有机化合物中,金属的价电子和配体提供或共享的电子总数等于18)。
(1) M的元素符号为 ;B的化学式为 。
(2) 写出上述所有核化学反应方程式。
(3) 写出B将Cr(Ⅲ)氧化为CrO42-的离子方程式。
(4) H2S代替H2O进行光合作用的主要产物是 ,该反应能够发生的主要原因是: 。
(5) 指出M2(CO)9中共有几种不同的成键方式,画出M2(CO)9的结构式。
 (2011?上海)实验室制取少量溴乙烷的装置如右图所示.根据题意完成下列填空:
(2011?上海)实验室制取少量溴乙烷的装置如右图所示.根据题意完成下列填空:| 加热 |
| 加热 |
 ?
?
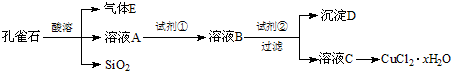
(1)在实验室用集气瓶收集气体G和气体H。则收集气体G的方法是 ,检验气体H已收集满的方法是 。?
(2)在实验室进行操作①时,除了使用酒精灯、铁架台、铁圈及夹持仪器外,还缺少的玻璃仪器是 ,在进行操作②时,应在HCl的气氛中加热脱水,其目的是 。?
(3)F位于元素周期表第? ?周期? ?族,写出其最高价氧化物对应的水化物的电子式? ?。写出反应A+H2O→B+H的化学方程式 。?
(4)某学生设计如图15-38装置,将产生的气体H通入硫酸铜溶液,制得深蓝色溶液J。现有下列?试剂?:?
 ?
?
图15-38
①稀NaOH溶液 ②H2O2溶液 ?③浓氨水 ?④NH4Cl?溶液 ⑤生石灰 ?⑥消石灰 ⑦碳酸氢钠?
(Ⅰ)a中的试剂:固体X应是? ?(填序号),溶液Y应是 (填序号)。
(Ⅱ)你认为使用装置b时存在的主要缺点: (用简明文字叙述)。?
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
| 80a-135b |
| 18b |
| 80a-135b |
| 18b |
| H2SO4 |
| NH3?H2O |
| △ |
| NH3?H2O |
| H2SO4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com