
题目列表(包括答案和解析)
(1)下列叙述正确的是( )
A.电能是二次能源 B.水力是二次能源
C.天然气是一次能源 D.焦炉气是一次能源
(2)关于用水制取二次能源氢气,以下研究方向不正确的是( )
A.构成水的氢和氧都是可以燃烧的物质,因此可以研究在水不分解的情况下,使氢气成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放出能量
D.寻找特殊化学物质,用以开发廉价能源,以分解水制取氢气
 目前有人提出理想的氢能源循环体系,类似于光合作用,太阳能和水是取之不尽、用之不竭,而且价格低廉的重要资源.按照如图所示的循
目前有人提出理想的氢能源循环体系,类似于光合作用,太阳能和水是取之不尽、用之不竭,而且价格低廉的重要资源.按照如图所示的循| A、制备大量燃料电池 | B、研发氢氧发电机 | C、将海水提纯 | D、研发合适光分解催化剂,使之在光照下促进水的分解速率加快 |
 2H2↑+O2↑
2H2↑+O2↑ 2H2↑+O2↑
2H2↑+O2↑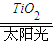 2H2↑+O2↑
2H2↑+O2↑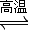 CO+3H2
CO+3H2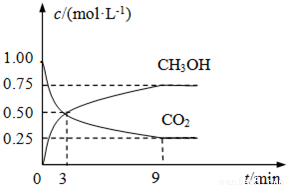
| 温度/℃ | 100 | 200 | 300 | 400 | |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
(8分)中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O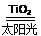 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O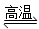 CO+3H2
CO+3H2
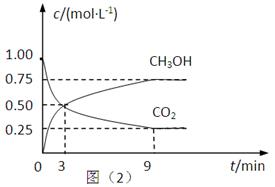
(2)CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化如上图所示。
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1,测得CO2和CH3OH(g)的浓度随时间变化如上图所示。
①从3 min到9 min,v(H2)=________mol·L-1·min-1。
②能说明上述反应达到平衡状态的是____________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g) CH3OH(g)的平衡常数:
CH3OH(g)的平衡常数:
|
温度/℃ |
0 |
100 |
200 |
300 |
400 |
|
平衡常数 |
667 |
13 |
1.9×10-2 |
2.4×10-4 |
1×10-5 |
下列说法正确的是_____。
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高
△H=517.6kJ/mol。根据以上叙述,回答下题:
下列叙述正确的是( )
A.电能是二级能源 B.水力是二级能源
C.天然气是一级能源 D.焦炉气是一级能源
已知:CH4(g)+2O2(g)══2H2O(1)+CO2(g),△H=-890.3kJ/mol,1g氢气和1g CH4分别燃烧后,放出的热量之比约为( )
A.1︰3.4 B.1︰1.7 C.2.3︰1 D.4.6︰1
关于用水制取二级能源氢气,以下研究方向正确的是( )
A.构成H2O的氢和氧都是可燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源
B.设法将太阳光聚焦,产生高温,使水分解产生H2
C.寻找高效催化剂,使水分解产生H2,同时释放能量
D.寻找特殊化学物质,用于开发廉价能源,以分解水制取H2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com