
题目列表(包括答案和解析)
| 试管序号 | 1 | 2 | 3 | 4 | 5 |
| 通入CO2时间/min | 0 | 1 | 5 | ||
| 滴加盐酸/滴 | 0 | 3 | 6 | ||
| 溶液中颜色对比 | 无色 | 浅黄色→黄色(依次加深) | |||
| 滴加淀粉溶液后的颜色对比 | 无色 | 浅蓝色→蓝色(依次加深) | |||
| 实验步骤 | 预期现象和结论 |
| ①取一份纯净的KI固体,分成两等份; | / |
| ②一份加入到装有 一份加入到装有 ③几天后观察. |
| 污染指数 | 首要污染物 | 空气质量等级 | 空气质量状况 |
| 55 | SO2 | Ⅱ | 良 |

| A、加入少量的H2SO4,使乙酸乙酯水解 | B、将浓H2SO4滴入萤石中加热 | C、将碘化氢通入浓H2SO4中 | D、将潮湿的氯气通过盛有浓H2SO4的洗气瓶中 |
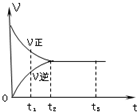 右图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
右图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com