
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
√∏∂‘–Ì∂ýªØ—ß∑¥”¶º∞…˙ŒÔÃ⁄µƒ∏¥‘”µƒ∑¥”¶æþ”–∫Ыøµƒ¥þªØ–ßπ˚°£œ¬¡–≤ª «√∏¥þªØÀ˘æþ”–µƒÃÿµ„µƒ «
A£ÆÃıº˛Œ¬∫Õ°¢≤ª–˺”»»
B£Æ≤ª лГ∫À·ºÓ∂»£®pH£©µƒ”∞œÏ
C£Æ∏þ∂»µƒ◊®“ª–‘
D£Æ∏þ–ßµƒ¥þªØ–‘
£®1£©œ¬¡– µ—È≤Ÿ◊˜ªÚ∂‘ µ—È ¬ µµƒ– ˆ÷–¥Ê‘⁄¥ÌŒÛµƒ «____________£®ÃÓ–Ú∫≈£©°£
A.”√50 mLÀ· ΩµŒ∂®πÐ◊º»∑¡ø»°25.00 mL KMnO4À·–‘»Ð“∫£¨∑≈»Î◊∂–Œ∆ø÷–¥˝”√
B.‘⁄≤‚∂®¡ÚÀ·Õ≠æßõƒΩ·æßÀÆ∫¨¡ø ±£¨Ω´◊∆…’¡ÚÀ·Õ≠æßõƒ€·€ˆ∑≈‘⁄ø’∆¯÷–¿‰»¥£¨»ª∫Û≥∆¡ø
C.÷–∫Õ»»µƒ≤‚∂®À˘–˵ƒ≤£¡ß“«∆˜”–…’±≠°¢Œ¬∂»º∆°¢¡øÕ≤
D. µ—È “÷–Ω¯––µƒœ¬¡– µ—Èæ˘–ËÀÆ‘°º”»»£∫
¢Ÿ±ΩµƒœıªØ∑¥”¶ ¢⁄∆œÃ—뵃“¯æµ∑¥”¶ ¢€““À·““ı•µƒ÷∆±∏ ¢ÐµÌ∑€°¢œÀŒ¨ÀÿµƒÀÆΩ‚
E.≈‰÷∆1 mol°§L-1µƒNaOH»Ð“∫ ±£¨œ¬¡–≤Ÿ◊˜æ˘ª·‘Ï≥…À˘≈‰≈®∂»∆´µÕ£∫¢Ÿ»ÐΩ‚∫Û…’±≠Œ¥∂ý¥Œœ¥µ” ¢⁄∂®»ð ±—ˆ ”øÃ∂»œþ ¢€»ð¡ø∆ø÷–‘≠”–…Ÿ–Ì’Ù¡ÛÀÆ
F. µ—È “≈‰÷∆¬»ªØ—«Ã˙»Ð“∫ ±£¨Ω´¬»ªØ—«Ã˙œ»»ÐΩ‚‘⁄—ŒÀ·÷–£¨»ª∫Û”√’Ù¡ÛÀÆœ° Õ≤¢º”»Î…Ÿ¡øÃ˙∑€
£®2£©ƒ≥Õ¨—߅˺∆¡À»ÁÕºÀ˘ æ≤‚∂®∫Ï¡◊‘⁄¬»∆¯÷–»º…’≤˙ŒÔµƒ∑÷◊” Ωµƒ◊∞÷√£¨∏√◊∞÷√÷–B «µ◊√ʪ˝Œ™100 cm2µƒ‘≤Õ≤◊¥≤£¡ß»ð∆˜£®√Ð∑‚∏«…œ◊∞”–∑ß√≈£©£¨…œ√ʱ͔–¿Â√◊µ•ŒªµƒøÃ∂»£¨∆‰À˚º–≥÷◊∞÷√“—¬‘»•°££®≤ªøº¬«ø…ƒÊ∑¥”¶£©
≤Ÿ◊˜≤Ω÷Ë£∫
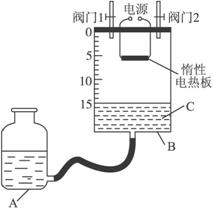
¢ŸºÏ≤È◊∞÷√µƒ∆¯√Ж‘
¢⁄Ω´0.5 g∫Ï¡◊∆Ω∆Ñ⁄µÁ»»∞Â…œ£¨∏«ΩÙ»ð∆˜
¢€¥Úø™∑ß√≈1°¢∑ß√≈2£¨¥”Aµƒ∆øø⁄º”»Î“∫ÃÂC£¨ πB÷–“∫√Ê÷¡øÃ∂»15.0 cm
¢ÐœÚB÷–≥‰»Î¬»∆¯£¨¥˝¬»∆¯≥‰¬˙∫Ûπÿ±’∑ß√≈1°¢∑ß√≈2£¨Õ®µÁº”»»∫Ï¡◊°≠°≠
«Îªÿ¥œ¬¡–Œ £∫
£®i£©ºÏ≤È◊∞÷√∆¯√Ж‘æþÃÂ∑Ω∑® «____________________°£
£®ii£© µ—È≤Ω÷Ë¢€º”»Îµƒ“∫ÃÂC «____________£®ÃÓ√˚≥∆£©°£
£®iii£©∑¥”¶Ω· ¯≤¢≥‰∑÷¿‰»¥∫Û£¨∂¡»°B÷–“∫√ÊøÃ∂»∂¡ ˝ ±£¨”¶◊¢“‚________________________£ª»Ù“∫√Ê‘⁄øÃ∂»5.6 cm¥¶£¨¥À ± µ—ÈÃıº˛Ω¸À∆ø¥◊˜±Í◊º◊¥øˆ£¨‘Ú…˙≥…ŒÔPClx÷–xµƒ÷µ «____________£®º∆À„Ω·π˚±£¡Ù1Œª–° ˝£©°£
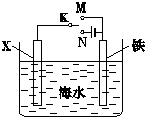 £®1£©¿˚”√»ÁÕº◊∞÷√£¨ø…“‘ƒ£ƒ‚Ã˙µƒµÁªØ—ß∑¿ª§£Æ»ÙXŒ™Ãº∞Ù£¨Œ™ºıª∫Ã˙µƒ∏Ø ¥£¨ø™πÿK”¶∏√÷√”⁄
£®1£©¿˚”√»ÁÕº◊∞÷√£¨ø…“‘ƒ£ƒ‚Ã˙µƒµÁªØ—ß∑¿ª§£Æ»ÙXŒ™Ãº∞Ù£¨Œ™ºıª∫Ã˙µƒ∏Ø ¥£¨ø™πÿK”¶∏√÷√”⁄| µ—È∑Ω∑® | µ—Èœ÷œÛº∞Ω·¬€ |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com