
题目列表(包括答案和解析)
Cu(OH)2在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
A、2 B、3 C、4 D、5
室温时,M(OH)2(s) M2+(aq)+2OH-(aq) Ksp=a。c(M2+)=b mol·L-1时,溶液的pH等于(?? )
M2+(aq)+2OH-(aq) Ksp=a。c(M2+)=b mol·L-1时,溶液的pH等于(?? )
A. lg(
lg( )? ?????????? B.
)? ?????????? B. lg(
lg(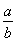 )
)
C.14+ lg(
lg( )???? ? ? D.14+
)???? ? ? D.14+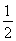 lg(
lg( )
)
Cu(OH)2在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
| A.2 | B.3 | C.4 | D.5 |
|
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.该电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”.高铁电池的总反应为: 3Zn+2K2FeO4+8H2O 下列叙述不正确的是 | |
| [ ] | |
A. |
放电时正极反应为: |
B. |
充电时阴极反应为:Zn(OH)2+2e-=Zn+2OH- |
C. |
放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
D. |
标有“+”的接线柱充电时作阳极,放电时作正极 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com