
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈЙВ16ЗжЃЉАДвЊЧѓЛиД№ЯТСаЮЪЬт
ЃЈ1ЃЉгУРызгЗНГЬЪННтЪЭДПМюШмвКШЅГ§гЭЮлЕФдвђЃК
ЃЈ2ЃЉаДГіХнФУ№Л№ЦїжаЗДгІЕФРызгЗНГЬЪН[ФквКЃКAl2(SO4)3 ЃЌЭтвКЃКNaHCO3]ЃК
ЃЈ3ЃЉSOCl2ЪЧвЛжжвКЬЌЛЏКЯЮяЃЌЗаЕуЮЊ77ЁцЁЃЯђЪЂга10mLЫЎЕФзЖаЮЦПжаЃЌаЁаФЕЮМг8~10ЕЮSOCl2 ,ПЩЙлВьЕНОчСвЗДгІЃЌвКУцЩЯгаАзЮэЩњГЩЃЌВЂгаЮоЩЋгаДЬМЄадЦјЮЖЦјЬхвнГіЃЌИУЦјЬхжаКЌгаЪЙЦЗКьШмвКЭЪЩЋЕФSO2ЃЌИљОнЪЕбщЯжЯѓЃЌаДГіSOCl2гыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЃК
еєИЩAlCl3ШмвКВЛФмЕУЕНЮоЫЎAlCl3ЃЌЪЙSOCl2гыAlCl3ЁЄ6H20ЛьКЯВЂМгШШЃЌПЩЕУЕНЮоЫЎAlCl3ЃЌНтЪЭдвђЃК
ЃЈ4ЃЉвбжЊЃКЧІаюЕчГизмЕФЛЏбЇЗНГЬЪНЮЊЃКPb+PbO2 +2H2SO4 2PbSO4+2H2O
ЂйЧІаюЕчГидкЗХЕчЪБИКМЋЗДгІЮЊ ЃЌ
ЂкЧІаюЕчГидкГфЕчЪБбєМЋЗДгІЮЊ ЃЛ
ЂлШчЙћЧІаюЕчГидкЗХЕчЪБЛиТЗжага2molЕчзгзЊвЦЪБЃЌЯћКФH2SO4 molЁЃ
ЃЈ5ЃЉГЃЮТЯТ,ШчЙћШЁ0.1mol/L HAШмвКгы0.1mol/L NaOHШмвКЕШЬхЛ§ЛьКЯ(КіТдЛьКЯКѓШмвКЬхЛ§ЕФБфЛЏ),ВтЕУЛьКЯШмвКЕФpH=8ЃЌЧѓГіЛьКЯвКжаЯТСаЫуЪНЕФОЋШЗМЦЫуНсЙћЃЈЬюОпЬхЪ§зжЃЉЃК
c(OHЃ)Ѓc(HA)ЃН ___________ mol/LЁЃ
ЃЈЙВ16ЗжЃЉАДвЊЧѓЛиД№ЯТСаЮЪЬт
ЃЈ1ЃЉгУРызгЗНГЬЪННтЪЭДПМюШмвКШЅГ§гЭЮлЕФдвђЃК
ЃЈ2ЃЉаДГіХнФУ№Л№ЦїжаЗДгІЕФРызгЗНГЬЪН[ФквКЃКAl2(SO4)3ЃЌЭтвКЃКNaHCO3]ЃК
ЃЈ3ЃЉSOCl2ЪЧвЛжжвКЬЌЛЏКЯЮяЃЌЗаЕуЮЊ77ЁцЁЃЯђЪЂга10mLЫЎЕФзЖаЮЦПжаЃЌаЁаФЕЮМг8~10ЕЮSOCl2 ,ПЩЙлВьЕНОчСвЗДгІЃЌвКУцЩЯгаАзЮэЩњГЩЃЌВЂгаЮоЩЋгаДЬМЄадЦјЮЖЦјЬхвнГіЃЌИУЦјЬхжаКЌгаЪЙЦЗКьШмвКЭЪЩЋЕФSO2ЃЌИљОнЪЕбщЯжЯѓЃЌаДГіSOCl2гыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЃК
еєИЩAlCl3ШмвКВЛФмЕУЕНЮоЫЎAlCl3ЃЌЪЙSOCl2гыAlCl3ЁЄ6H20ЛьКЯВЂМгШШЃЌПЩЕУЕНЮоЫЎAlCl3ЃЌНтЪЭдвђЃК
ЃЈ4ЃЉвбжЊЃКЧІаюЕчГизмЕФЛЏбЇЗНГЬЪНЮЊЃКPb+PbO2 +2H2SO4  2PbSO4+2H2O
2PbSO4+2H2O
ЂйЧІаюЕчГидкЗХЕчЪБИКМЋЗДгІЮЊ ЃЌ
ЂкЧІаюЕчГидкГфЕчЪБбєМЋЗДгІЮЊ ЃЛ
ЂлШчЙћЧІаюЕчГидкЗХЕчЪБЛиТЗжага2molЕчзгзЊвЦЪБЃЌЯћКФH2SO4 molЁЃ
ЃЈ5ЃЉГЃЮТЯТ,ШчЙћШЁ0.1mol/L HAШмвКгы0.1mol/L NaOHШмвКЕШЬхЛ§ЛьКЯ(КіТдЛьКЯКѓШмвКЬхЛ§ЕФБфЛЏ),ВтЕУЛьКЯШмвКЕФpH=8ЃЌЧѓГіЛьКЯвКжаЯТСаЫуЪНЕФОЋШЗМЦЫуНсЙћЃЈЬюОпЬхЪ§зжЃЉЃК
c(OHЃ)Ѓc(HA)ЃН ___________ mol/LЁЃ
ЃЈЙВ16ЗжЃЉАДвЊЧѓЛиД№ЯТСаЮЪЬт
ЃЈ1ЃЉгУРызгЗНГЬЪННтЪЭДПМюШмвКШЅГ§гЭЮлЕФдвђЃК
ЃЈ2ЃЉаДГіХнФУ№Л№ЦїжаЗДгІЕФРызгЗНГЬЪН[ФквКЃКAl2(SO4)3 ЃЌЭтвКЃКNaHCO3]ЃК
ЃЈ3ЃЉSOCl2ЪЧвЛжжвКЬЌЛЏКЯЮяЃЌЗаЕуЮЊ77ЁцЁЃЯђЪЂга10mLЫЎЕФзЖаЮЦПжаЃЌаЁаФЕЮМг8~10ЕЮSOCl2 ,ПЩЙлВьЕНОчСвЗДгІЃЌвКУцЩЯгаАзЮэЩњГЩЃЌВЂгаЮоЩЋгаДЬМЄадЦјЮЖЦјЬхвнГіЃЌИУЦјЬхжаКЌгаЪЙЦЗКьШмвКЭЪЩЋЕФSO2ЃЌИљОнЪЕбщЯжЯѓЃЌаДГіSOCl2гыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЃК
еєИЩAlCl3ШмвКВЛФмЕУЕНЮоЫЎAlCl3ЃЌЪЙSOCl2гыAlCl3ЁЄ6H20ЛьКЯВЂМгШШЃЌПЩЕУЕНЮоЫЎAlCl3ЃЌНтЪЭдвђЃК
ЃЈ4ЃЉвбжЊЃКЧІаюЕчГизмЕФЛЏбЇЗНГЬЪНЮЊЃКPb+PbO2 +2H2SO4  2PbSO4+2H2O
2PbSO4+2H2O
ЂйЧІаюЕчГидкЗХЕчЪБИКМЋЗДгІЮЊ ЃЌ
ЂкЧІаюЕчГидкГфЕчЪБбєМЋЗДгІЮЊ ЃЛ
ЂлШчЙћЧІаюЕчГидкЗХЕчЪБЛиТЗжага2molЕчзгзЊвЦЪБЃЌЯћКФH2SO4 molЁЃ
ЃЈ5ЃЉГЃЮТЯТ,ШчЙћШЁ0.1mol/L HAШмвКгы0.1mol/L NaOHШмвКЕШЬхЛ§ЛьКЯ(КіТдЛьКЯКѓШмвКЬхЛ§ЕФБфЛЏ),ВтЕУЛьКЯШмвКЕФpH=8ЃЌЧѓГіЛьКЯвКжаЯТСаЫуЪНЕФОЋШЗМЦЫуНсЙћЃЈЬюОпЬхЪ§зжЃЉЃК
c(OHЃ)Ѓc(HA)ЃН ___________ mol/LЁЃ
ЁО16ЗжЁПНёгаФГбЇЩњЩшМЦЕФгУДпЛЏбѕЛЏЗЈжЦШЁЩйСПHNO3ШмвКЕФЪЕбщзАжУЃЌШчЯТЭМЫљЪОЁЃ
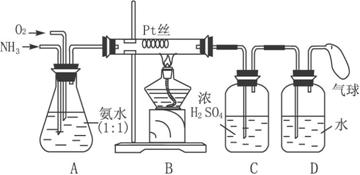
ЧыЛиД№ЯТСаЮЪЬтЁЃ
(1)ЪЕбщЪвжЦБИNH3ЃЌЯТСаЗНЗЈжавЫбЁгУЕФЪЧ________(ЬюађКХ)
ЂйЙЬЬЌТШЛЏяЇгыЪьЪЏЛвЛьКЯМгШШ
ЂкЙЬЬЌТШЛЏяЇМгШШЗжНт
ЂлЩњЪЏЛвжаЕЮМгХЈАБЫЎ
ЂмТШЛЏяЇШмвКгыЧтбѕЛЏФЦШмвКЙВШШ
(2)зАжУBжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______________ЃЛдкЪЕбщЙ§ГЬжаЃЌМгШШPtЫПКьШШКѓЃЌвЦШЅОЦОЋЕЦЃЌЗЂЯжPtЫПЛЙМЬајБЃГжКьШШЃЌгЩДЫПЩХаЖЯИУЗДгІЪЧ_____________________ЁЃ
(3)зАжУCЕФзїгУЪЧ__________ЃЛзАжУCжаЕФЯжЯѓЪЧ__________ЃЛЮЊШЗБЃDжаОЁПЩФмЖрЩњГЩHNO3ЃЌЫљЭЈШыO2КЭNH3ЕФЬхЛ§БШгІДѓгк__________ЁЃ
(4)АБдкИпЮТЯТДпЛЏбѕЛЏЪБЛЙгаИБЗДгІЗЂЩњЃК4NH3+3O2![]() 2N2+6H2OЁЃШєКіТдзАжУжаВаСєЕФЦјЬхЬхЛ§ЃЌВтЕУDжага1.0 molЁЄL-1ЕФHNO3ШмвК150 mLЃЌЦјЧђжаЪеМЏЕФЛьКЯЦјЬхЬхЛ§ЮЊ400 mL(БъзМзДПі)ЃЌЦфжаNO2ЁЂO2гыN2ЕФЬхЛ§БШЮЊ2ЁУ2ЁУ1ЃЌдђбѕЛЏГЩNOЕФАБеМБЛбѕЛЏЕФЬхЛ§ЗжЪ§ЮЊ_________ЁЃ
2N2+6H2OЁЃШєКіТдзАжУжаВаСєЕФЦјЬхЬхЛ§ЃЌВтЕУDжага1.0 molЁЄL-1ЕФHNO3ШмвК150 mLЃЌЦјЧђжаЪеМЏЕФЛьКЯЦјЬхЬхЛ§ЮЊ400 mL(БъзМзДПі)ЃЌЦфжаNO2ЁЂO2гыN2ЕФЬхЛ§БШЮЊ2ЁУ2ЁУ1ЃЌдђбѕЛЏГЩNOЕФАБеМБЛбѕЛЏЕФЬхЛ§ЗжЪ§ЮЊ_________ЁЃ
ЃЈБОЬтЙВ16ЗжЃЉЗРжЮЛЗОГЮлШОЪЧЕБЧАЛЗБЃЙЄзїЕФживЊбаОПФкШнжЎвЛЁЃЖўбѕЛЏСђКЭЕЊбѕЛЏЮяЪЧДѓЦјЕФжївЊЮлШОЮяЁЃ
1ЃЎНЋ1.5 mol SO2гУЧтбѕЛЏФЦШмвКЁЂЪЏЛвМАбѕЦјДІРэКѓЃЌМйЩшСђдЊЫиВЛЫ№ЪЇЃЌРэТлЩЯПЩЕУЕН_________________gЪЏИрЃЈCaSO4•2H2OЃЉЁЃ
2ЃЎгУCH4ЯћГ§NOxЮлШОЕФЛЏбЇЗНГЬЪНЮЊЃК
CH4ЃЋ4NO Ёњ 2N2ЃЋCO2ЃЋ2H2OЃЛ CH4ЃЋ2NO2 Ёњ N2ЃЋCO2ЃЋ2H2O
Яжга11.2 L NO2ЁЂNOЕФЛьКЯЦјЬхNOxЃЌНЋЦфЛЙдЮЊN2ЃЌашвЊ4.48 L ЕФCH4ЃЌдђЛьКЯЦјЬхжаNO2ЁЂNOЕФЮяжЪЕФСПЗжБ№ЮЊ___________________ЁЃЃЈЬхЛ§ЖМвбЛЛЫуЮЊБъзМзДПіЃЉ
3ЃЎЃЈ1ЃЉГЃЮТЯТгУбѕШБЮЛЬњЫсаПZnFe2OyПЩвдЯћГ§NOxЮлШОЃЌЪЙNOxзЊБфЮЊN2ЃЌЭЌЪБZnFe2OyзЊБфЮЊZnFe2O4ЁЃШє2 mol ZnFe2OyгызуСПNO2ПЩЩњГЩ0.5mol N2ЃЌдђyЃН_______________ЁЃ
ЃЈ2ЃЉбѕШБЮЛЬњЫсаПZnFe2OzЛЏбЇЪНЕФбѕЛЏЮяаЮЪНЮЊaZnO•bFeO•cFe2O3ЁЃвбжЊ1 mol ZnFe2OzзюЖрФмЪЙ4.0 LЃЈБъПіЃЉNO1.4зЊЛЏЮЊN2ЁЃдђЩЯЪібѕЛЏЮяаЮЪНЕФЛЏбЇЪНПЩОпЬхБэЪОЮЊ______________________________ЁЃ
4ЃЎЕЭЮТГєбѕбѕЛЏЭбСђЭбЯѕММЪѕПЩвдЭЌЪБЮќЪебЬЦјжаЕФЕЊбѕЛЏЮяКЭЖўбѕЛЏСђЃЌЗДгІдРэЪЧНЋNOxбѕЛЏГЩN2O5ЃЌЭЈЙ§ЯДЕгаЮГЩЯѕЫсбЮЃЌЖўбѕЛЏСђаЮГЩСђЫсбЮЁЃЦфжївЊЗДгІШчЯТЃК
NOЃЋO3 Ёњ NO2ЃЋO2 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЂй
2NO2ЃЋO3 Ёњ N2O5ЃЋO2 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЂк
N2O5ЃЋ2NH3ЃЋH2OЁњ 2NH4NO3 ЁЁЁЁЁЁЁЁЁЁЁЁЂл
SO2ЃЋO3ЃЋ2NH3ЃЋH2O Ёњ (NH4)2SO4ЃЋO2 ЁЁЁЁЁЁЁЁЂм
ФГШШЕчГЇбЬЦјжаЦНОљКЌNOx 4.5ЁыЁЂSO29.0Ёы(ЬхЛ§ЗжЪ§)ЃЌбЙЫѕПеЦјОГєбѕЗЂЩњЦїБфГЩГєбѕПеЦјЃЌЦфжаO3ХЈЖШЮЊ90 L/m3ЃЌГєбѕПеЦјгыМгЪЊАБЦјКЭбЬЦјЛьКЯЗДгІЁЃШєСїСПБШЮЊyЃЌЧыЭЈЙ§МЦЫуСаГіyгыxЕФЙиЯЕЪНЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com