
题目列表(包括答案和解析)
| 元素代号 | 相关信息 |
| A | A与C可形成A2C和A2C2两种化合物 |
| B | B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D的单质能与冷水剧烈反应,得到强碱溶液 |
| E | 在第3周期元素中,E的简单离子半径最小 |
| 元素代号 | 相关信息 |
| A | A与C可形成A2C和A2C2两种化合物 |
| B | B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D的单质能与冷水剧烈反应,得到强碱溶液 |
| E | 在第3周期元素中,E的简单离子半径最小 |
| 元素代号 | 相关信息 |
| A | A与C可形成A2C和A2C2两种化合物 |
| B | B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙 |
| C | C的原子最外层电子数是其内层电子数的三倍 |
| D | D的单质能与冷水剧烈反应,得到强碱溶液 |
| E | 在第3周期元素中,E的简单离子半径最小 |
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |

硫代硫酸钠(Na2S2O3)俗称保险粉,可用作定影剂,也可用于纸浆漂白、脱氯剂等。
Na2S2O3易溶于水,不溶于乙醇,常温下溶液中析出晶体通常为Na2S2O·5H2O。实验室制备保险粉的装置如下图所示。涉及的总化学方程式如下: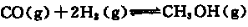
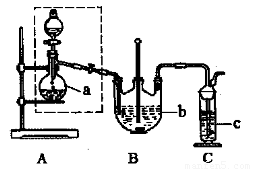
(1)检查虚线框内装置气密性的方法是? ????????????? 。
(2)反应前仪器a中加入的药品为???????? ,仪器c中加入的药品为 ?????????? 。
(3)仪器b的名称是?????????? 。
(4)在制备过程中,持续通人气体时,观察到B装置中先有大量浅黄色沉淀析出,反应一段时间,沉淀逐渐减少;待浅黄色沉淀消失时反应完成,停止加热。反应的离子方程式为??????? ???????????????? 。
(5)反应完成后,为了从混合溶液中获取产品,操作如下:
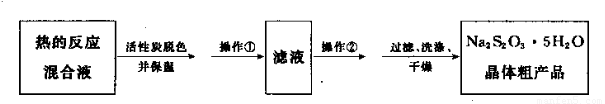
操作②为????????????? 。
(6)为了测产品的纯度,称取8.000 g粗产品,配制成250 mL溶液,用移液管移取25.00 mL于锥形瓶中,再用0.05000 mol·L-l的碘标准溶液进行滴定(2S2O32-+I2=S4O62-+2I-),
平行3次实验,平均消耗碘标准溶液的体积为30.00mL。
①测得产品的纯度为????????? 。
②关于上述实验的有关操作,以下表述正确的是 ??????????? 。(填编号)
A.用碱式滴定管盛装碘标准溶液
B.用移液管移取25.00mL溶液于锥形瓶中,移液管的尖嘴和锥形瓶内壁要接触
C.如果滴定终点没有控制好,碘标准溶液滴加过量,则必须重新进行滴定
D.滴定过程中若剧烈摇动锥形瓶(溶液不外溅),则所测得的纯度将会偏高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com