
题目列表(包括答案和解析)
某无色溶液中含有K+、Cl-、OH-、SO![]() 、SO
、SO![]() ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液.检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示.
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液.检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示.

(1)图中试剂②~④溶质的化学式分别是:②________,③________,④________.
(2)图中现象a、c表明检验出的离子分别是:
a________、c________.某无色溶液中含有K+、Cl-、OH-、SO![]() 、SO
、SO![]() ,为检验溶液中所含
,为检验溶液中所含
的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试
液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。

(1)图中试剂①~⑤溶质的化学式分别是:
①_________,②_________,③_________,④_________,⑤_________。
(2)图中现象a、b、c表明检验出的离子分别是:
a_________、b_________、c_________。
(3)白色沉淀A加试剂②反应的离子方程式是___________________________________
__________________。
(4)无色溶液C加试剂③的主要目的是_____________________________________。
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是
________________________________________________________________________。
(6)气体E通入试剂④发生反应的离子方程式是__________________________________。
(11分)某无色溶液中含有K+、Cl-、OH-、、
,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
请你根据实验操作及现象分析完成下列各题:
(1)图中现象a、b、c表明检验出的阴离子分别是:
a_________________, b___________________,c_____________________。
(2)白色沉淀A加过量试剂②发生反应的离子方程式是:___________________。
(3)无色溶液A加试剂③的主要目的是:_____________________________________。
(4)白色沉淀A若加试剂③而不加试剂②对实验结果有无影响(选填“有影响”、“无影响"或“无法确定”)____________________________。
(5)气体B通入试剂④中发生反应的离子方程式是:____________________________。
(11分)某无色溶液中含有K+、Cl-、OH-、 、
、 ,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
请你根据实验操作及现象分析完成下列各题:
(1)图中现象a、b、c表明检验出的阴离子分别是:
a_________________, b___________________,c_____________________。
(2)白色沉淀A加过量试剂②发生反应的离子方程式是:___________________。
(3)无色溶液A加试剂③的主要目的是:_____________________________________。
(4)白色沉淀A若加试剂③而不加试剂②对实验结果有无影响(选填“有影响”、“无影响"或“无法确定”)____________________________。
(5)气体B通入试剂④中发生反应的离子方程式是:____________________________。
某无色溶液中含有K+,Cl-,OH-,SO32-,SO42-,为了检验除OH-外的其它所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氢氧化钡溶液、溴水和酚酞六种试剂,设计如下实验步骤,并记录相关现象:
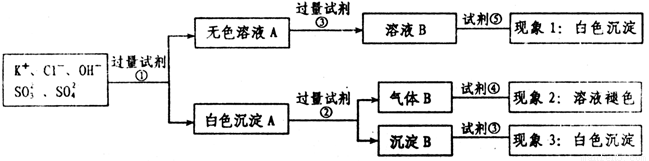 下列有关结论错误的是 (
)
下列有关结论错误的是 (
)
A.试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl
B.现象3中白色沉淀是BaSO4
C.试剂②是盐酸,试剂③是硝酸
D.产生现象2的离子方程式是:Br2+2H2O+SO2=4H++2Br-+SO42-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com