
题目列表(包括答案和解析)
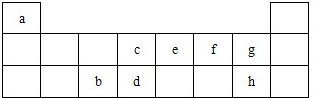 表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12∶1,B的相对分子质量为78。回答下列问题:
(1)A的电子式_______,A的结构简式_______。
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式_______________________________________________,反应类型________。
(3)在碘水中加入B振荡静置后的现象________________。
(4)B与浓硫酸与浓硝酸在50~60℃反应的化学反应方程式__________________________,反应类型________。
(5)等质量的A、B完全燃烧时消耗O2的物质的量______(填“A>B”、“A<B”或“A=B”)。
(1)人类的生活和生产活动,可以说都离不开能源。在 ①石油、②电能、③风能、④煤、⑤天然气、⑥秸杆、⑦水力、⑧水煤气这些能源中,属于“二级能源”的是 ;属于“不可再生能源”的是 。(填序号)
(2)甲、乙两种金属: ①甲单质能与乙盐的溶液反应; ②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙; ③分别与氯气反应生成金属阳离子时,甲失去电子数比乙多;④甲、乙两元素的单质和盐酸组成原电池,乙单质表面生成氢气。其中一定能说明甲的金属性比乙强的有 。(填序号)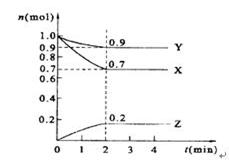
(3)某温度时,在2 L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示。由图中所给数据进行分析,该反应的化学方程式为 ;反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= ;反应达到平衡时,Y的浓度为 。
(1)人类的生活和生产活动,可以说都离不开能源。在 ①石油、②电能、③风能、④煤、⑤天然气、⑥秸杆、⑦水力、⑧水煤气这些能源中,属于“二级能源”的是 ;属于“不可再生能源”的是 。(填序号)
(2)甲、乙两种金属: ①甲单质能与乙盐的溶液反应; ②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙; ③分别与氯气反应生成金属阳离子时,甲失去电子数比乙多;④甲、乙两元素的单质和盐酸组成原电池,乙单质表面生成氢气。其中一定能说明甲的金属性比乙强的有 。(填序号)

(3)某温度时,在2 L的密闭容器中,X、Y、Z的物质的量随时间的变化曲线如图所示。由图中所给数据进行分析,该反应的化学方程式为 ;反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= ;反应达到平衡时,Y的浓度为 。
(1)人类的生活和生产活动,可以说都离不开能源。在 ①石油、②电能、③风能、④煤、⑤天然
气、⑥秸杆、⑦水力、⑧水煤气这些能源中,属于“二级能源”的是_ _ __ ;属于
“不可再生能源”的是___ _。(填序号)
(2)甲、乙两种金属: ①甲单质能与乙盐的溶液反应; ②甲、乙两元素原子的最外层电子数
相同,且甲的原子半径小于乙; ③分别与氯气反应生成金属阳离子时,甲失去电子数比乙多;
④甲、乙两元素的单质和盐酸组成原电池,乙单质表面生成氢气。其中一定能说明甲的金属性比
乙强的有 。(填序号)
(3)某温度时,在2 L的密闭容器中,X、Y、Z的物质的
量随时间的变化曲线如图所示。由图中所给数据进行分析,
该反应的化学方程式为 ;
反应从开始至2分钟末,用Z的浓度变化表示的平均反应速
率为v(Z)= ;反应达到平衡时,Y的浓度为 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com