
题目列表(包括答案和解析)
(08深圳宝安区一模)由两种短周期元素A和M形成的离子化合物A2M3,A3+离子比M2-离子少一个电子层,且A3+具有与Ne原子相同的核外电子层结构,则下列说法正确的是()
A、化合物A2M3是三氧化二铝
B、A3+和M2-最外电子层上的电子数都是8
C、A的最高价氧化物对应的水化物是强电解质
D、元素M是第2周期第VIA族的元素
(08深圳宝安区一模)下列说法中,不正确的是 ()
A. 在NaAlO2溶液中,HSO3-(H2SO3的电离常数K1=1.5×10-2;K2=1.0×10-7)不可能大量存在
B. 在0.1mol?L-1的氢溴酸中加入适量的蒸馏水,溶液的c(H+)减小
C. 在由水电离出的c(
D. 室温下pH=6的酸性溶液中,可能存在NH3?H2O分子
(08深圳宝安区一模)常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如下图所示:
 |
回答下列问题:
(1)20mL 0.1mol/LNa2CO3溶液呈碱性的原因是(用离子方程式表示): ;其溶液中所有阳离子和阴离子的浓度有何关系?(用等式表示) 。
(2)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确 。
(3)若向20mL 0.1mol/LNa2CO3溶液中加入BaCl2粉末3.328×10-7g时开始产生沉淀X,则KSP(X)= 。
(4)当加入盐酸使溶液PH为10时,混合液中含碳元素的离子有哪些? ,其物质的量之比为 。
(5)请写出OAB段的离子方程式 ;当混合液的PH= 时,开始放出CO2气体。
(08深圳宝安区一模)下列离子方程式正确的是()
A.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+ H2O
B.澄清石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O
C.在NaOH溶液中通人少量的SO2气体:SO2+OH―=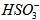
D.碳酸钡中加入稀硫酸:BaCO3+2H+=Ba2++CO2↑+H2O
(08深圳宝安区一模)从宏观方面来说物质由元素组成,从微观方面来说物质由粒子构成。下列说法中不正确的是()
A. 互为同位素
互为同位素
B.只由一种分子组成的物质一定为纯净物
C.质子数等于电子数的某微粒,可能是一种分子或一种离子
D.46gNO2和46gN2O4含有的原子数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com