
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЯТСаСНжжЦјЬхЕФЗжзгЪ§вЛЖЈЯрЕШЕФЪЧ( )
A.жЪСПЯрЕШЁЂУмЖШВЛЕШЕФN2КЭC2H4 B.ЕШЬхЛ§ЁЂЕШУмЖШЕФCOКЭC2H4
C.ЕШЮТЁЂЕШЬхЛ§ЕФO2КЭN2 D.ЕШбЙЁЂЕШЬхЛ§ЕФN2КЭCO2
етЕРЬтдДгкШЫУёНЬг§ГіАцЩчЛЏбЇНЬВФЕквЛВс53вГЕкЖўДѓЬтЕк5ЬтЃЌдЬтШчЯТЃК
дкЯрЭЌЬѕМўЯТЃЌЯТСаЦјЬхжаЫљКЌЗжзгЪ§ФПзюЖрЕФЪЧ( )
A.1 g H2 B.10 g O2 C.30 g Cl2 D.17 g NH3
ЩЯЪіСНЬтОљЮЊБШНЯЪ§ФПЗжзгЕФЁЃПЮБОЬтФПжиЕуПМВщЛљБОЙЋЪНЃКN=nNAЃЌn=m/MЁЃИпПМЬтдкБОЬтЛљДЁЩЯНјааСЫЭиеЙЃЌжиЕуПМВщАЂЗќМгЕТТоЖЈТЩМАЦфЭЦТлЁЃВЛТлдѕбљПМВщЃЌДѓМвМЧзЁЦјЬхЮяжЪЕФСПЕФДѓаЁОіЖЈЗжзгЪ§ЕФЖрЩйМДПЩЁЃ
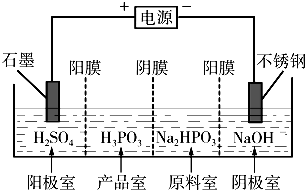 ЃЈ2013?МУФўЖўФЃЃЉбЧСзЫсЃЈH3PO3ЃЉЪЧЖўдЊЫсЃЌH3PO3ШмвКДцдкЕчРыЦНКтЃКH3PO3?H++H2PO3-ЃЎбЧСзЫсгызуСПNaOHШмвКЗДгІЃЌЩњКЭNa2HPO3ЃЎ
ЃЈ2013?МУФўЖўФЃЃЉбЧСзЫсЃЈH3PO3ЃЉЪЧЖўдЊЫсЃЌH3PO3ШмвКДцдкЕчРыЦНКтЃКH3PO3?H++H2PO3-ЃЎбЧСзЫсгызуСПNaOHШмвКЗДгІЃЌЩњКЭNa2HPO3ЃЎ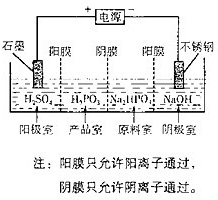 ЃЈ2013?ЙужнвЛФЃЃЉбЧzЫсЃЈH3PO3ЃЉЪЧЖўдЊЫсЃЌгызуСПNaOHШмвКЗДгІЩњГЩNa2HPO3ЃЎ
ЃЈ2013?ЙужнвЛФЃЃЉбЧzЫсЃЈH3PO3ЃЉЪЧЖўдЊЫсЃЌгызуСПNaOHШмвКЗДгІЩњГЩNa2HPO3ЃЎ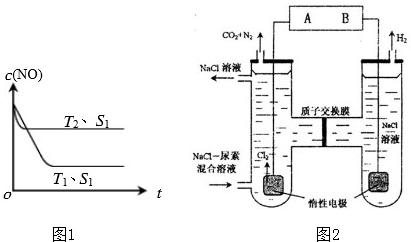 ЦћГЕЮВЦјвбГЩЮЊживЊЕФПеЦјЮлШОЮяЃЎ
ЦћГЕЮВЦјвбГЩЮЊживЊЕФПеЦјЮлШОЮяЃЎ| ЪЕбщзщ | ЮТЖШЁц | Ц№ЪМСП/mol | ЦНКтСП/mol | ДяЕНЦНКтЫљаш ЪБМф/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
| a |
| b |
SO2ЪЧв§Ц№ДѓЦјЮлШОЕФжївЊгаКІЦјЬхжЎвЛЃЌЮвЙњДѓЦјжЪСПБъзМжаЙцЖЈДѓЦјжаSO2ЕФзюИпХЈЖШЯожЕШчЯТБэЃКДѓЦјжаSO2Ш§МЖБъзМХЈЖШЯожЕ
| ХЈЖШЯожЕ[mg/(m3ПеЦј)] | |||
| вЛМЖБъзМ | ЖўМЖБъзМ | Ш§МЖБъзМ | |
| ФъШеЦНОљ | 0.02 | 0.06 | 0.10 |
| ШеЦНОљ | 0.05 | 0.15 | 0.25 |
| ШЮКЮвЛДЮ | 0.15 | 0.50 | 0.70 |
зЂЃКЁАФъШеЦНОљЁБЮЊШЮКЮвЛФъЕФЦНОљХЈЖШОљжЕВЛаэГЌЙ§ЕФЯожЕЃЛЁАШеЦНОљЁБЮЊШЮКЮвЛШеЕФЦНОљХЈЖШВЛаэГЌЙ§ЕФЯожЕЃЛЁАШЮКЮвЛДЮЁБЮЊШЮКЮвЛДЮВЩбљВтЖЈВЛаэГЌЙ§ЕФХЈЖШЯожЕЁЃ
ОнБЈЕРЃЌ1952Фъ2дТЃЌФГГЧЪаЮэДѓЮоЗчЃЌМвЭЅКЭЙЄГЇХХГіЕФбЬЮэООУВЛЩЂЃЌДѓЦјжаSO2ЕФКЌСПИпДя3.8mg/ЃЈm3ПеЦјЃЉ ЃЌбЬГОДя4.5mg/ЃЈm3ПеЦјЃЉЃЌОгУёНЁПЕЦеБщЪмЕНЮЃКІЃЌ4ЬьжЎФкЫРЭіШЫЪ§дМ4000ЃЌСїОИУГЧЪаЕФжївЊКгЕРвВвђДЫЖјЪмЕНЮлШОЃЌв§Ц№гуРрЫРЭіЁЃДѓЦјжаЕФSO2НЋжБНгЮЃКІТНЩњИпЕШжВЮяЕФ____зщжЏЃЌДѓЦјжаSO2ГЌБъзюШнвзгАЯьШЫЕФ_______ЯЕЭГЖјЛММВВЁЃЌЖјКгСїжагуРрЫРЭігыSO2дьГЩДѓЦјЮлШОЫљаЮГЩ______гаЙиЁЃ
ФГПеЦјЮлШОМрВтвЧЪЧИљОнSO2КЭBr2ЫЎЕФЖЈСПЗДгІРДВтЖЈПеЦјжаЕФSO2КЌСПЕФЁЃЗДгІЕФфхРДздвЛИізАгаЫсадЃЈЯЁСђЫсЃЉЕФKBrШмвКЕФЕчНтГибєМЋЕФбѕЛЏЗДгІЃЌЕчНтГиЕФбєМЋЪвгывѕМЋЪвЪЧИєПЊЕФЁЃЕБВтСПФГЕиЧјПеЦјжаSO2ЕФКЌСПЪБЃЌвЛЬьжазїСЫШ§ДЮШЁбљМрВтЃЌУПДЮШЁбљЕФПеЦјЃЈвбГ§ГОЃЉЖМвд1.5ЁС10-4m3.min-1ЕФСїЫйНјШыЕчНтГиЕФбєМЋЪвЃЌДгЕчСїМЦЯдЪОГіУПДЮЕФЕчСїЧПЖШЗжБ№ЮЊ8.56ЁС10-6AЁЂ9.25ЁС10-6A ЁЂ8.12ЁС10-6AЃЌУПДЮЖМФмЙЛБЃГжЕчНтГижаBr2ХЈЖШКуЖЈВЂЧЁКУгыЖўбѕЛЏСђЭъШЋЗДгІЃЈЩшПеЦјжаВЛКЌгыфхЗДгІЕФЦфЫќдгжЪЁЂ1ИіЕчзгЕчСПЮЊ1.6ЁС10-19CЃЉЁЃ
аДГіДЫМрВтЙ§ГЬжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЁЃМЦЫуИУЕиЧјПеЦјжаЖўбѕЛЏСђЕФКЌСПгаУЛгаДяЕНДѓЦјжЪСПБъзМЃП
ЕБДѓЦјжаSO2ЮлШОНЯбЯжиЪБЃЌФПЧАгавЛжжНЕЕЭЦфЮЃКІЕФЗНЗЈЪЧгУжБЩ§ЗЩЛњХчШіАзлбЗлЃЌЦфЛЏбЇЗНГЬЪНЮЊ___________________ЁЃ
ФГЛ№СІЗЂЕчГЇЫљдкЕигаНЯЗсИЛЕФЬМЫсИЦПѓКЭСтУОПѓЃЌШєИУЗЂЕчГЇвдКЌСђжигЭзїШМСЯЃЌЧыОЭЕиШЁВФЬсГіШ§жжЛЏбЇЗДгІдРэгыЩЯвЛаЁЬтВЛЭЌЕФЁАЭбСђЁБЗНЗЈЃЈгУЛЏбЇЗНГЬЪНБэЪОЃЌЃЉЃК
ЕквЛжж______________ЃЛЕкЖўжж______________ЃЛ ЕкШ§жж______________ЁЃ
ФГ10 6 kWЛ№СІЗЂЕчГЇвджигЭЮЊШМСЯЁЃвдКЌСђ3.5%ЕФжигЭЮЊШМСЯЃЌжигЭЪЙгУСПЮЊ0.18 dm3.kW-1.h-1ЃЈжигЭЕФУмЖШЮЊ0.95g.cm3ЃЉЁЃИУГЇПЊЙЄТЪЃЈУПФъЪЕМЪдЫзЊЬьЪ§ЃЉЮЊ80%ЃЌЖдбЬЕРЦјЕФЭбСђаЇТЪЮЊ90%ЁЃЮЪвЛФъМфЖдбЬЕРЦјЭбСђЛиЪеЕФSO2ФмЩњГЩЖрЩйЖжЪЏИрЃЈCaSO4ЁЄ2H2OЃЉЃП
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com