
题目列表(包括答案和解析)
大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的有________(填字母).
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g+2H2O(g) ΔH2=-1160 kJ·mol-1
2N2(g)+CO2(g+2H2O(g) ΔH2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为________.
(3)脱碳.将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH3
CH3OH(g)+H2O(g) ΔH3
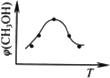
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数![]() (CH3OH)与反应温度T的关系曲线如图所示,则上述CO2转化为甲醇的反应的ΔH3________0(填“>”、“<”或“=”).
(CH3OH)与反应温度T的关系曲线如图所示,则上述CO2转化为甲醇的反应的ΔH3________0(填“>”、“<”或“=”).
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如下图所示.下列说法正确的是________(填字母代号).

A.第10 min后,向该容器中再充入1 mol CO2和3 mol H2,则再次达到平衡时C(CH3OH)=1.5 mol/L
B.0~10 min内,氢气的平均反应速率为0.075 mol/(L·min)
C.达到平衡时,氢气的转化率为75%
D.该温度下,反应的平衡常数的值为3/16
E.升高温度将使n(CH3OH)/n(CO2)减小
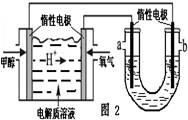
③有学者设想以下图所示装置用电化学原理将CO2转化为重要化工原料.若A为CO2,B为H2,C为CH3OH,则正极电极反应式为________.

(4)脱硫.某种脱硫工艺中将废气经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.硫酸铵和硝酸铵的水溶液的pH<7,其中原因可用一个离子方程式表示为:________;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中[Na+]+[H+]________[NO3-]+[OH-](填写“>”“=”或“<”)
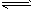 CH3OH(g)+H2O(g) △H<0。若容器容积不变,充入1 mol CO2和3 mol H2后,下列措施可增加甲醇产率的是____。
CH3OH(g)+H2O(g) △H<0。若容器容积不变,充入1 mol CO2和3 mol H2后,下列措施可增加甲醇产率的是____。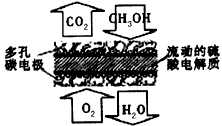
(15分)火力发电厂释放出大量氮氧化物(NOx)、SO2和CO2等气体会造成环境问题。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g) + 4NO2(g) =4NO(g) + CO2(g) + 2H2O(g) △H1=-574 kJ·mol-1
CH4(g) + 4NO(g) =2N2(g) + CO2(g) + 2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3

①在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图1所示。回答:0~10 min内,氢气的平均反应速率为 mol/(L·min);第10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡 (填“正向”、“逆向”或“不”)移动。
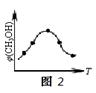
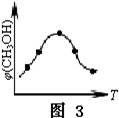
②取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇的反应的△H3 0(填“>”、“<”或“=”)。
(3)脱硫。利用Na2SO3溶液可脱除烟气中的SO2。Na2SO3可由NaOH溶液吸收SO2制得。NaOH溶液吸收SO2的过程中,pH随n(SO32-)︰n(HSO3﹣)变化关系如下表:
| n(SO32﹣)︰n(HSO3﹣) | 91︰9 | 1︰1 | 9︰91 |
| pH | 8.2 | 7.2 | 6.2 |
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
| n(SO32﹣)︰n(HSO3﹣) | 91︰9 | 1︰1 | 9︰91 |
| pH | 8.2 | 7.2 | 6.2 |
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3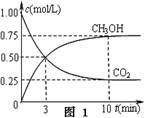
必考卷
第Ⅰ卷共18小题,每小题6分,共108分。
一、选择题:选对的给6分,选错的得0分。
1.B 2.B 3.C 4.B 5.A
6.B 7.D 8.A 9.C 10.D 11.C 12.A
二、选择题:全部选对的给6分,选对但不全的给3分,有选错的得0分。
13.D 14.B 15.B C 16. A 17.AD 18.D
.files/image102.gif) 第Ⅱ卷共9题,共161分。
第Ⅱ卷共9题,共161分。
19.(18分)
(1)13.85 (5分)
.files/image103.gif) (2)① (4分)
(2)① (4分)
测量电路如图所示 (5分)
② 建议一:多测几组R、U数据,分别列方
程组求出E、r,再求出E、r平均值。
建议二:多测几组R、U数据,分别求出
相应的Ⅰ值,用U、Ⅰ数据作出U―Ⅰ图
线,由图线的截距、斜率求出E、r。
其他建议合理的同样给分。 (4分)
因电表选错导致①不能得分的,第②题可参照评分标准酌情给分。
20.(15分)
运动员从开始滑下至c点,由机械能守恒定律得
.files/image105.gif) ①
(5分)
①
(5分)
运动员滑至最低点时,由牛顿运动定律和向心力公式得
.files/image107.gif) ② (5分)
② (5分)
由①②得 .files/image109.gif) ③
③
代入已知数据,求得 .files/image111.gif) ④ (5分)
④ (5分)
21.(19分)
21.(1)设硬橡胶块与塑料盖恰好分离时,两者的共同速度为.files/image113.gif) ,从开始滑动到分离经历时间为t,在此期间硬橡胶块与塑料盖的加速度大小分别为a1、a2 ,由牛顿第二定律得:
,从开始滑动到分离经历时间为t,在此期间硬橡胶块与塑料盖的加速度大小分别为a1、a2 ,由牛顿第二定律得:
.files/image115.gif) ① (2分)
① (2分)
.files/image117.gif) ②
(2分)
②
(2分)
.files/image119.gif) ③ (2分)由以上各式得
③ (2分)由以上各式得
.files/image121.gif) ④ (2分)
④ (2分)
(2)设硬橡胶块与塑料盖恰好分离时,硬橡胶块移动的位移为.files/image123.gif) ,取硬橡胶块分析,应用动能定理得
,取硬橡胶块分析,应用动能定理得 .files/image125.gif) ⑤(3分)
⑤(3分)
由系统能量关系可得 .files/image127.gif) ⑥(3分)
⑥(3分)
由④⑤⑥式可得
.files/image129.gif) ⑦(3分)
⑦(3分)
因 .files/image131.gif) ,故硬橡胶块将落入污水井内 (2分)
,故硬橡胶块将落入污水井内 (2分)
.files/image132.gif) 22.(20分)
22.(20分)
(1)带电粒子从A点射入磁场区域后,由牛顿运
动定律和向心力公式得
.files/image134.gif) ① (2分)
① (2分)
∴ .files/image136.gif) ② (2分)
② (2分)
.files/image137.gif) (2)粒子运动轨迹如图1所示。 (6分)
(2)粒子运动轨迹如图1所示。 (6分)
(3)由①式得带电粒子运动速率 .files/image139.gif) ,即v与r成正比。
,即v与r成正比。
由题意可知,该粒子从A点射入磁场区域又不离开磁场外边界的最小可能轨道半径(如图2)
.files/image141.gif) ③ (4分)
③ (4分)
由此可得粒子从A点射入磁场区域又不离开磁场
外边界的允许的最大速率
.files/image143.gif) ④ (2分)
④ (2分)
∴ .files/image145.gif) ⑤ (2分)
⑤ (2分)
代入数据解得 .files/image147.gif) ⑥ (2分)
⑥ (2分)
23.(15分)
[探究一]
(1) 2NaA1O2+3H2↑ (3分)
(或 2Na[A1(OH)4]+3H2↑)
(2)偏高 (2分)
[探究二]
(1)不需要 (2分)
(2)检查装置的气密性(或合金完全溶解,或加入足量盐酸,或调整
量气管C的高度,使C中液面与B液面相平等合理答案) (3分)
[探究三]
(1)灼烧后固体的质量 (3分)
(2)是 (2分)
24.(15分)
(1)淀粉(或糖类、葡萄糖、油脂等合理答案) (1分)
(2)CH4 (1分)
O2 + 2H2O + 4e- = 4OH- (3分)
(3)该盐是硝酸铵,发生水解反应:NH4++H2O.files/image149.jpg) NH3•H2O
+H+,
NH3•H2O
+H+,
溶液呈酸性 (3分)
c(NO3-)> c(NH4+) > c(H+) > c(OH-) (3分)
(4)HCO3- + H+ H2O + CO2↑
(3分)
氨基乙酸(或甘氨酸) (1分)
25.(15分)
(1)SO3 +
H2O H2SO4
(3分)
(2)①< ②C (各3分,共6分)
(3)B (3分)
(4)根据SO2 ~ CaSO4•2H2O
.files/image151.jpg) (3分)
(3分)
26.(25分)
Ⅰ.
(1)①适量(一定浓度的)KOH溶液 (2分)
②(一定浓度的)葡萄糖溶液、微生物悬浮液各1mL (2分)
③测定细胞呼吸CO2释放量与O2消耗量的差值 (2分)
(2)④只进行有氧呼吸(进行有氧呼吸和产生乳酸的无氧呼吸) (2分)
⑤只进行产生酒精和CO2的无气氧呼吸 (2分)
⑥进行有氧呼吸和产生酒精、CO2的无氧呼吸 (2分)
(3)(任答一项,或其它合理答案) (3分)
①测定小麦种子的呼吸速率
②测定玉米幼苗的光合作用强度
③探究小麦幼苗、玉米幼苗光合作用强度的差异
Ⅱ.
(1)① ③ (各2分,共4分)
(2)④、⑤ (2分)
下丘脑分泌促甲状腺释放激素(TRH)和垂体分泌促
甲状腺激素(TSH) (2分)
(3)亢进 (2分)
27.(15分)
(1)存在生殖隔离 (3分)
(2)性状分离(高酚性状的植株);非同源 (各3分,共6分)
(3)用甲与乙杂交,得到F1;F1自交,获得F2,从中选出抗黄萎病、
抗虫植株继续自交,期望下代获得抗黄萎病、抗虫纯合体 (6分)
或:
|