
题目列表(包括答案和解析)
(6分)模型是研究化学的一种方法,例如原子结构示意图、电子式、分子结构模型等,可以帮助我们开启化学思维。下图是两种常见的有机物分子结构模型,回答有关问题:
(1)甲所代表的物质空间构型是 。
(2)乙所代表的物质中碳碳键的特点是: 。
(3)在化学学习中,你还学习过哪些化学模型 (答出一种即可)。
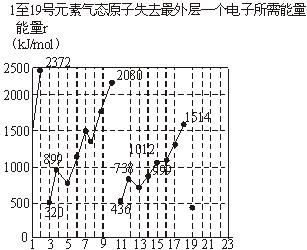
(1)同主族内不同元素的E值变化的特点是: 。各主族中E值的这种变化特点体现了元素性质的 变化规律。
(2)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象,试预测下列关系式中正确的是 (填写编号,多选倒扣)。
①E(砷)>E(硒) ②E(砷)<E(硒)
③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1 mol气态Ca原子失去最外层一个电子所需能量E值的范围:
<E< 。
(4)10号元素E值较大的原因是 。
A.无色透明 B.一定温度范围逐渐软化
C.没有固定的熔点 D.加热后具有流动性
铅玻璃常用于制作光学玻璃,因为其具有的特点是( )
A.膨胀系数小 B.折光率强
C.耐酸耐高温 D.化学稳定性好
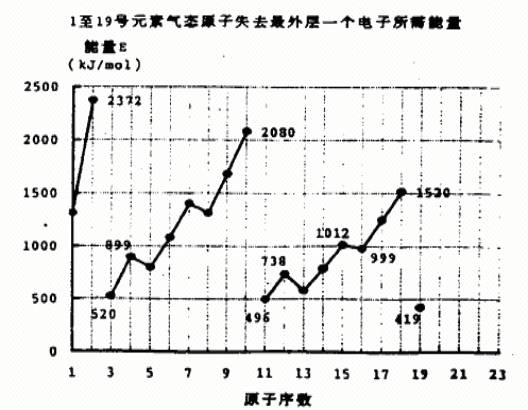
⑴ 同主族内不同元素的E值变化的特点是: 。各主族中E值的这种变化特点体现了元素性质的 变化规律。
⑵ 同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常现象。试预测下列关系中正确的是 (填写编号,多选倒扣)
① E(砷)>E(硒) ②E(砷)<E(硒)
③ E(溴)>E(硒) ④E(溴)<E(硒)
⑶ 估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围: <E<
⑷ 10号元素E值较大的原因是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com