
题目列表(包括答案和解析)

T℃时,A气体和B气体反应生成C气体。反应过程中A、B、C浓度变化如下图甲所示,若保持其它条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如下图乙所示,则下列结论正确的是
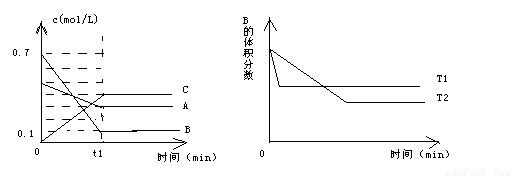
甲 乙
A.t1min时,保持其它条件不变,增大压强,平衡向逆反应方向移动
B.t1min时,保持容器总体积不变,通入少量稀有气体,平衡向逆反应方向移动
C.其它条件不变时,升高温度,正、逆反应速率均增大,且A的转化率减小
D. T℃时,在相同容器中,若有1.0mol/L A、1.4mol/L B开始反应,达到平衡后,C的浓度等于0.8mol/L
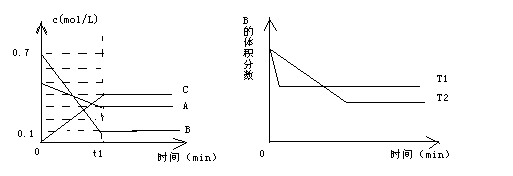
T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )

A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
C.T℃时,在相同容器中保持容积不变,若由0.3mol?L―1 A、0.1 mol?L―1 B和0.4 mol?L―1 C开始反应,达到平衡后,C的浓度仍为0.4 mol?L―1
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
一、单项选择题(45分)
1.D 2.B 3.A 4.C 5.B 6.B 7.C 8.A 9.D 10.B 11.C 12.B 13.D 14.D 15.A
二、(27分
16.(6分)(1)0.05mol?L-1?s-1 (2分)
(2)0.05mol(2分) (3).files/image291.gif) (2分)
(2分)
17.(9分)(1)碱(1分).files/image293.gif) (2分
(2分
(2).files/image295.gif) (2分,只写离子符号不得分)
(2分,只写离子符号不得分)
(3)④ ⑤ ③ ② ①(2分)
(4)NAOH完全电离(1分),.files/image030.gif) 水解是可逆反应,反应进行不彻底(1分)
水解是可逆反应,反应进行不彻底(1分)
18.(12分)(1).files/image298.gif)
.files/image300.gif)
.files/image112.gif)
.files/image303.gif) (各1分,写物质名称也可给分)
(各1分,写物质名称也可给分)
(2).files/image305.gif) =====
=====.files/image307.gif) (3分)
(3分)
.files/image309.gif) =====
=====.files/image311.gif) (3分)
(3分)
(3) .files/image313.gif)
.files/image108.gif) (2分,各1分)
(2分,各1分)
三、(22分)19.(11分)(1).files/image316.gif)
.files/image318.gif)
.files/image320.gif) (2分)
(2分)
.files/image322.gif)
.files/image261.gif) (2分,各1分)红棕色褪去(1分) 加成(1分)
(2分,各1分)红棕色褪去(1分) 加成(1分)
(2)分液漏斗(1分).files/image325.gif) (2分)
(2分)
(3).files/image326.gif) (2分)
(2分)
20.(11分)(1)铁丝在氯气中燃烧,生成棕黄色的烟(3分)
黄(2分) 抑制.files/image328.gif) 水解(3分),答防止
水解(3分),答防止.files/image328.gif) 水解扣1分)
水解扣1分)
(2).files/image330.gif) =====
=====.files/image332.gif) (3分)
(3分)
四、(6分)21.(6分)0.75mol?L-1或0.95 mol?L-1(各3分)
B卷
五、(16分)
22.C 23.D 24.D 25.B 26.C 27.A 28.D 29.B
六、(28分)30.(4分)(1).files/image334.gif) +
+ .files/image336.gif) =====
===== .files/image338.gif) (2分)
(2分)
(2).files/image340.gif) =====
===== .files/image342.gif) (2分)
(2分)
31.(8分)(1).files/image344.gif)
.files/image346.gif)
.files/image046.gif) (3分,各1分,有错扣1分)
(3分,各1分,有错扣1分)
.files/image349.gif) 或
或.files/image351.gif) (2分,其他合理答案也可给分)
(2分,其他合理答案也可给分)
(2).files/image353.gif) (1分)
(1分).files/image355.gif) 第一步电离产生的
第一步电离产生的.files/image245.gif) 抑制了
抑制了.files/image346.gif) 的电离(2分)
的电离(2分)
32.(4分)(1)A (2分) (2)5:4 (2分)
33.(12分)(1).files/image112.gif) (2分) 受热分解生成
(2分) 受热分解生成.files/image360.gif) (2分) c点(2分)
(2分) c点(2分)
得到较高温度水蒸气(1),并排出装置中残留的空气,防止铁粉被氧化(1)
(2).files/image280.gif) ====
====.files/image363.gif) (2分)
(2分)
.files/image365.gif) =====
=====.files/image367.gif) (2分)
(2分)
七、(6分)34.(6分)(1)10:1(2分) (2)2(2分) (3)101:9 (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com