
题目列表(包括答案和解析)

| ||
| ||


 F (g)+D (g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F (g)+D (g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)A、B、C、D、E是短周期元素组成的中学常见的物质,存在如图所示的转化关系(部分生成物和反应条件略去)

(1)若C为二氧化碳,则A可能为___________________;
(2)若X为金属单质,则X与B的稀溶液反应生成C的
离子方程式为___________________________;
(3)若D为白色沉淀,与A摩尔质量相等,则A为_________,反应③的离子方程式为 ____________;
(4)若A为无色液体,且B、E的摩尔质量相等,反应①的化学方程式为_____________;
(5)若A为一氧化碳,则D为____________;t ℃时,在2 L的密闭的容器中加入3 mol CO和0.75 mol 水蒸气,达到平衡时,CO的转化率为20%,在相同温度下再加入3.75 mol 水蒸气,再次达到平衡时,能否计算出CO的转化率? 。若能,请计算;若不能,请说明理由。

A、B、C、D、E是短周期元素组成的中学常见的物质,存在如图所示的转化关系(部分生成物和反应条件略去)
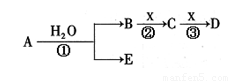
(1)若C为二氧化碳,则A可能为___________________;
(2)若X为金属单质,则X与B的稀溶液反应生成C的
离子方程式为___________________________;
(3)若D为白色沉淀,与A摩尔质量相等,则A为_________,反应③的离子方程式为 ____________;
(4)若A为无色液体,且B、E的摩尔质量相等,反应①的化学方程式为_____________;
(5)若A为一氧化碳,则D为____________;t ℃时,在2 L的密闭的容器中加入3 mol CO和0.75 mol 水蒸气,达到平衡时,CO的转化率为20%,在相同温度下再加入3.75 mol 水蒸气,再次达到平衡时,能否计算出CO的转化率? 。若能,请计算;若不能,请说明理由。

A、B、C、D、E是短周期元素组成的中学常见的物质,存在如图所示的转化关系(部分生成物和反应条件略去) 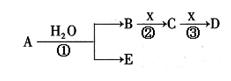
(1)若C为二氧化碳,则A可能为___________________;
(2)若X为金属单质,则X与B的稀溶液反应生成C的
离子方程式为___________________________;
(3)若D为白色沉淀,与A摩尔质量相等,则A为_________,反应③的离子方 程式为 ____________;
程式为 ____________;
(4)若A为无色液体,且B、E的摩尔质量相等,反应①的化学方程式为_____________;
(5)若A为一氧化碳,则D为____________;t ℃时,在2 L的密闭的容器中加入3 mol CO和0.75 mol 水蒸气,达到平衡时,CO的转化率为20%,在相同温度下再加入3.75 mol 水蒸气,再次达到平衡时,能否计算出CO的转化率? 。若能,请计算;若不能,请说明理由。
(16分) 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语
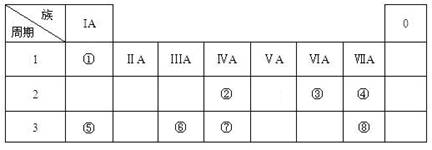
回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为_______________________,②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是______________________。
(2)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl 3 c.Na2SO3 d.KMnO4
若已知1 克该液态化合物分解成③的单质和一种常见液体时,可放出2.9kJ能量,写出该反应的热化学方程式:
(3)工业上常采用电解A和冰晶石(Na3AlF6)混合物的方法冶炼制备⑥的单质,请从A晶体的类型和微粒间的相互作用力角度解释加冰晶石(Na3AlF6)的原因 。 并写出电解时的电极反应式: 。
(4)甲、乙、丙是上述部分元素组成的双原子分子或负二价双原子阴离子,且甲、乙、丙的电子总数相等。甲是一种极强的氧化性单质。丙与⑤的阳离子可形成一种淡黄色固体B,该固体跟水反应可得到③的单质。则B电子式 ,乙的结构式 ,甲的组成元素的原子结构示意图 ,能证明甲的组成元素非金属性很强的事实 。(任举一例即可)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com