
题目列表(包括答案和解析)
| ||
| ||
M g二氧化锰与足量的浓盐酸完全反应:4HCl+MnO2![]() MnCl2+Cl2↑+2H2O生成V L气体(标准状况),则被氧化的HCl是
MnCl2+Cl2↑+2H2O生成V L气体(标准状况),则被氧化的HCl是
[ ]
A.![]() mol B.
mol B.![]() mol
mol
C.![]() g D.
g D.![]() g
g
| ||
| ||
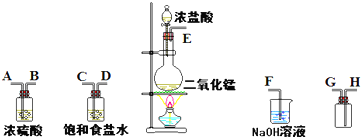
已知二氧化锰固体与浓盐酸共热可以生成氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,现有4.35g二氧化锰固体与足量的浓盐酸充分反应,转移电子的物质的量与被氧化的HCl的物质的量分别为
MnCl2+Cl2↑+2H2O,现有4.35g二氧化锰固体与足量的浓盐酸充分反应,转移电子的物质的量与被氧化的HCl的物质的量分别为
A.0.1mol;0.2mol B.0.2mol;0.1mol
C.0.2mol;0.2mol D.0.1mol;0.1mol
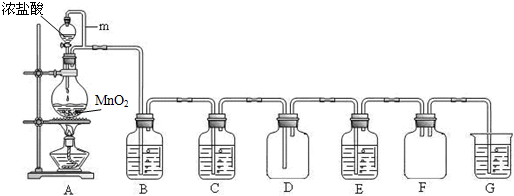
实验室用加热二氧化锰与浓盐酸的混合物制备氯气:
MnO2+4HCl(浓)一套完整的氯气实验室制备装置应该由四部分构成
(如图).同学们需要注意实验仪器的连接和作用.
A.分液漏斗:用来盛放液体试剂,本实验用来盛装浓盐酸.
B.圆底烧瓶:做反应容器,内放固体物质,本实验盛装的是固体二氧化锰.在加浓盐酸时要注意液体的量不能超过烧瓶容积的________,而且加热时要________,使烧瓶底部均匀受热,避免受热不均而炸裂.
C.除杂装置:第一个洗气瓶内盛有饱和食盐水,它的作用是除去氯气中混有的氯化氢杂质;第二个洗气瓶内盛有浓硫酸,用于除去氯气中混有的水蒸气.洗气瓶中两个导管的插入原则是“长进短出”.除杂的顺序是先除氯化氢,后除水蒸气.如果顺序颠倒,不能起到除杂的作用,原因是________.
D.集气装置:用来收集密度比空气大的气体要用向上排空气法.如果不需要收集干燥的氯气,也可以使用________的方法.
E.尾气吸收:因为氯气有毒,会污染环境,多余的氯气不能排放到大气中,选用________进行尾气处理.
一、选择题(本大题包括23小题,每小题3分,共69分。每小题只有一个正确选项)
1.C 2.B 3.C 4.A 5.C 6.A 7.C 8.B 9.D 10.C 11.D 12.B 13.B 14.C 15.A 16.A 17.A 18.D 19.D 20.B 21.A 22.D 23.C
二、(本大题包括2小题。共12分)
24.⑴无机非金属材料 陶瓷 白色污染
⑵原电池
(3)鲜鸡蛋 精面粉、白砂糖 精炼植物油 柠檬汁(每空1分,共8分)
25.(1)致密的氧化物保护膜 (2)②
(每空2分,共4分)
三、(本大题包括1小题。共7分)
26.⑴B 烧杯、漏斗、(3分)
⑵AgNO3溶液 稀HNO3
取少量固体与强碱溶液混合加热,生成的气体用湿润的红色石蕊试纸检验(3分)
⑶2NaHCO3 Na2CO3+CO2↑+H2O (1分)
Na2CO3+CO2↑+H2O (1分)
四、(本大题包括1小题。共5分)
27. (1) Na2O2(1分) Fe(OH)3(1分) (2)
五、(本大题包括1小题。共7分)
28. 0.25 mol?L-1 0.1 mol?L-1
注:主观性试题中出现的合理答案均给分。
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com