
题目列表(包括答案和解析)
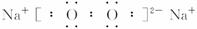
(1)A的分子式是___________,甲的电子式是___________。
(2)D的溶液与乙反应的离子方程式是__________________________。
(3)若1.7 g A与O2反应生成气态的B和C时放出22.67 kJ热量,写出该反应的热化学方程式:_______________________________________________________。
(10分)物质的转化关系如下图所示(有的反应可能在水溶液中进行)。
其中A为化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。
(1)若A为硫酸工业的重要原料,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3 溶液有白色沉淀生成。则:
①工业上反应Ⅱ在 中进行(填设备名称),工业上反应Ⅲ用于吸收E的试剂是 。
②D的水溶液呈 性(填“酸”、“碱”或“中”)。③反应I的化学方程式是 。
(2)若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。则
①甲的电子式是 。②写出B和甲反应的化学方程式是 。
③若17gA与O2反应生成气态的B和C时放出226.7kJ热量,写出该反应的热化学方程式: 。
物质的转化关系如下图所示(有的反应可能在水溶液中进行).其中甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成.请回答下列问题:
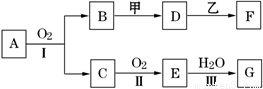
请回答些列问题:
(1)写出甲的电子式是 .
(2)写出反应Ⅰ的化学方程式 .
(3)A溶于水得到得到溶液X,在25℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为 用含a和b的代数式表示出该混合溶液中X的电离平衡常数 .
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0-6.0之间,通过如图装置处理污水.
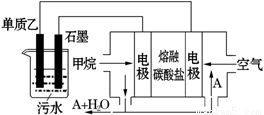
①电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ. ;Ⅱ. .
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图).A物质的化学式是 .
(10分)物质的转化关系如下图所示(有的反应可能在水溶液中进行)。
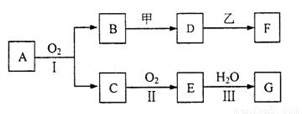
其中A为化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。
(1)若A为硫酸工业的重要原料,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3 溶液有白色沉淀生成。则:
①工业上反应Ⅱ在 中进行(填设备名称),工业上反应Ⅲ用于吸收E的试剂是 。
②D的水溶液呈 性(填“酸”、“碱”或“中”)。③反应I的化学方程式是 。
(2)若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。则
①甲的电子式是 。②写出B和甲反应的化学方程式是 。
③若17gA与O2反应生成气态的B和C时放出226.7kJ热量,写出该反应的热化学方程式: 。
物质的转化关系如下图所示(有的反应可能在水溶液中进行).其中甲为淡黄色固体化合物,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化,用两根玻璃棒分别蘸取化合物A、G的浓溶液并使它们接近,有大量白烟生成.请回答下列问题: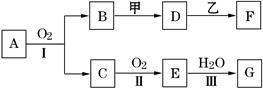
请回答些列问题:
(1)写出甲的电子式是 .
(2)写出反应Ⅰ的化学方程式 .
(3)A溶于水得到得到溶液X,在25℃下,将a mol·L-1的X与b mol·L-1的G溶液等体积混合,溶液显中性,则所得溶液中离子浓度由大到小的顺序为 用含a和b的代数式表示出该混合溶液中X的电离平衡常数 .
(4)工业上采用的一种污水处理方法是:保持污水的pH在5.0-6.0之间,通过如图装置处理污水.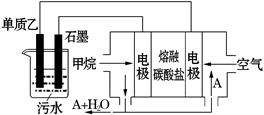
①电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是:Ⅰ. ;Ⅱ. .
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图).A物质的化学式是 .
题号
1
2
3
4
5
6
7
8
答案
C
A
A
B
C
D
B
B
题号
9
10
11
12
13
14
15
答案
C
D
B
B
B
C
D
16.(8分,每空两分)
H O
| ||
(1)HOCH2CH2―N―C―CH3
(2)②
NH2 O
| ||
(3)①CH3CH2CH―C―OH
NO2 NO2
| |
②CH3CH―CH2CH2CH3 CH3CH―CH(CH3)2
|