
题目列表(包括答案和解析)
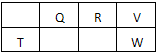




(1)Z2的电子式为______________,Y的原子结构示意图为______________。
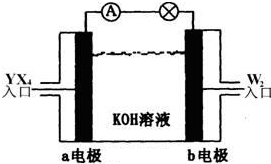
(2)将X2、W2按下图所示通入某燃料电池中,其中,b电极为______________极(填“正”或“负”),电极反应式为____________________________。
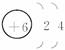
(3)X、Y两种元素组成一种气体,在标准状况下密度为
(4)由X、Y、Z、W四种元素组成的酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为_____________________________________________________________________。
有X、Y、Z、W四种短周期元素,原子序数依次增大.X的阳离子就是一个质子.Z、W在周期表内处于相邻位置,它们的单质在通常状况下均为无色气体.Y原子的最外层电子数是次外层电子数的2倍.请回答:
(1)Z2的电子式为________,Y的原子结构示意图为________.
(2)将X2、W2按下图所示通入某燃料电池中,其中,b电极为________极(填“正”或“负”),电极反应式为________.
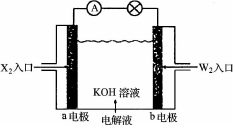
(3)X、Y两种元素组成一种气体,在标准状况下密度为1.25 g·L-1,实验室制取该气体的化学方程式为________.
(4)由X、Y、Z、W四种元素组成的酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为________.
| |||||||||||||||||||||||
题号
1
2
3
4
5
6
7
8
答案
C
A
A
B
C
D
B
B
题号
9
10
11
12
13
14
15
答案
C
D
B
B
B
C
D
16.(8分,每空两分)
H O
| ||
(1)HOCH2CH2―N―C―CH3
(2)②
NH2 O
| ||
(3)①CH3CH2CH―C―OH
NO2 NO2
| |
②CH3CH―CH2CH2CH3 CH3CH―CH(CH3)2
|