
题目列表(包括答案和解析)
(11分)以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取低碳醇的热力学数据:
反应I:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
反应II:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)
△H = —173.6 kJ·mol-1
CH3CH2OH(g)+3H2O(g)
△H = —173.6 kJ·mol-1
(1)写出由CH3CH2OH +_____ 2CH3OH的热化学方程式为:__________________。
2CH3OH的热化学方程式为:__________________。
(2)在一定条件下,对于反应I:在体积恒定的密闭容器中,达到平衡的标志是__ (填字母)
a.CO2和CH3OH 浓度相等 b.H2O的百分含量保持不变
c.H2的平均反应速率为0 d.v正(CO2)=3v逆(H2)
e.混合气体的密度不再发生改变
f. 混合气体的平均相对分子质量不再发生改变
如果平衡常数K值变大,该反应 (填字母)
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
其他条件恒定,如果想提高CO2的反应速率,可以采取的反应条件是 (填字母) ,
达到平衡后,想提高H2转化率的是_______________(填字母)
a、降低温度 b、补充H2 c、移去甲醇 d、加入催化剂
(3)在密闭容器中,对于反应II中,研究员以生产乙醇为研究对象,在5MPa、m= n(H2)/n(CO2)=3时,测得不同温度下平衡体系中各种物质的体积分数(y%)如图所示,则表示CH3CH2OH体积分数曲线的是 ;表示CO2的体积分数曲线的是 。
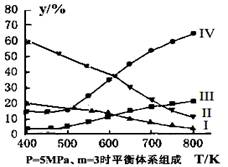
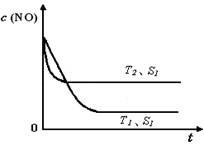
(4)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。上图是反应:2NO(g)
+ 2CO(g)
 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线, 若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线, 若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
(1)(6 分)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
aA (g)+ bB (g) 2C(g)
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则①a= ,b= ;
②2S内B的反应速率= 。
(2)(4分)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:
③有 个电子通过了电线?(NA=6.02×1023)
④此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
(3)(2分)将2.3g金属钠放入足量的mg重水(D2O)中,完全反应后,所得溶液中溶质的质量分数是 (用含m的代数式表示)。
(1)(6 分)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
aA (g)+ bB (g)  2C(g)
2C(g)
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则①a= ,b= ;
②2S内B的反应速率= 。
(2)(4分)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:
③有 个电子通过了电线?(NA=6.02×1023)
④此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
(3)(2分)将2.3g金属钠放入足量的mg重水(D2O)中,完全反应后,所得溶液中溶质的质量分数是 (用含m的代数式表示)。
(11分)以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取低碳醇的热力学数据:
反应I: CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1
反应II:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) △H =" —173.6" kJ·mol-1
CH3CH2OH(g)+3H2O(g) △H =" —173.6" kJ·mol-1
(1)写出由CH3CH2OH+_____ 2CH3OH的热化学方程式为:__________________。
2CH3OH的热化学方程式为:__________________。
(2)在一定条件下,对于反应I:在体积恒定的密闭容器中,达到平衡的标志是__ (填字母)
a.CO2和CH3OH 浓度相等 b.H2O的百分含量保持不变
c.H2的平均反应速率为0 d.v正(CO2)=3v逆(H2)
e.混合气体的密度不再发生改变
f. 混合气体的平均相对分子质量不再发生改变
如果平衡常数K值变大,该反应 (填字母)
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
其他条件恒定,如果想提高CO2的反应速率,可以采取的反应条件是 (填字母) ,
达到平衡后,想提高H2转化率的是_______________(填字母)
a、降低温度 b、补充H2 c、移去甲醇 d、加入催化剂
(3)在密闭容器中,对于反应II中,研究员以生产乙醇为研究对象,在5MPa、m= n(H2)/n(CO2)=3时,测得不同温度下平衡体系中各种物质的体积分数(y%)如图所示,则表示CH3CH2OH体积分数曲线的是 ;表示CO2的体积分数曲线的是 。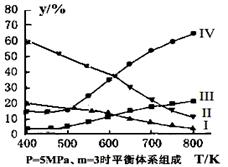
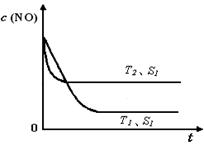
(4)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。上图是反应:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
(共12分)I.(6分)常压下乙醇的沸点为78.5℃,乙酸的沸点为118℃,以下是分离乙醇、乙酸的方案,请填空[(1)(3)是药品,(2)(4)是操作名称]
填空:(1) (3) (4)
|
回答下列问题:
(1)A装置中a仪器的名称________,b中盛放的物质是________(填化学式)。
(2)若去掉B装置会对什么元素的测量结果有影响? (填元素符号)
(3)E装置中所盛放物质最好选用________(选填:①氢氧化钙溶液 ②氢氧化钠溶液 ③水)
(4)若准确称取1.12g样品(样品只含C、H、O三种元素中的两种或三种)。经充分 燃烧后,D装置增重1.44g,E装置增重3.52g,则该有机物样品中所含的元素为________(填元素符号)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com