
题目列表(包括答案和解析)
用砂纸擦后的镁带丐沸水反应,再向反应后溶液中滴加酚酞溶液向新制的H2S饱和溶液中滴加新制的氯水钠与润滴有酚酞的冷水反应镁带与2mol·L-1盐酸反应铝条与2mol·L-1盐酸反应向ALCI3溶液中滴加NaOH溶液至过量
A. 浮于水面,熔成闪亮的小球,四边游动,逐渐缩小,溶液变红色
B. 产生大量的气体,气体可燃,溶液变浅红色
C. 反应+分剧烈,产生的气体可燃
D. 剧烈反应,产生的气体可燃
E. 生成白色胶状沉淀,继而沉淀消失
F. 生成淡黄色沉淀
(3)实验内容:
实验方案 实验现象 有关化学方程
(4)实验结论:________。
(5)问题讨论:①请从结构理论上简单说明上述结论的原因。
②请你补充一组实验方案(简单易行),证明此周期中另两种主族元素的性质递变规律。
现有下列短周期元素性质的数据:
元素编号
元素性质 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
原子半径
(10-10m) 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82
最高和最
低化合价 +2 +1 +5 +7 +1 +5 +3
-2 -3 -1 -3
试回答下列问题:
(1)上述元素中处于同一主族的有________,元素②在周期表中的位置为________。
(2)上表中某两种元素,形成的分子中,每个原子都满足最外层为8电子的稳定结构,写出其电子式________。
(3)元素①⑥能形成两种化合物,写出其中较稳定的化,合物与水反应的,离子方程式:________。
A. 浮于水面,熔成闪亮的小球,四边游动,逐渐缩小,溶液变红色
B. 产生大量的气体,气体可燃,溶液变浅红色
C. 反应+分剧烈,产生的气体可燃
D. 剧烈反应,产生的气体可燃
E. 生成白色胶状沉淀,继而沉淀消失
F. 生成淡黄色沉淀
(3)实验内容:
实验方案 实验现象 有关化学方程
(4)实验结论:________。
(5)问题讨论:①请从结构理论上简单说明上述结论的原因。
②请你补充一组实验方案(简单易行),证明此周期中另两种主族元素的性质递变规律。
现有下列短周期元素性质的数据:
元素编号
元素性质 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
原子半径
(10-10m) 0.74 1.60 1.52 1.10 0.99 1.86 0.75 0.82
最高和最
低化合价 +2 +1 +5 +7 +1 +5 +3
-2 -3 -1 -3
试回答下列问题:
(1)上述元素中处于同一主族的有________,元素②在周期表中的位置为________。
(2)上表中某两种元素,形成的分子中,每个原子都满足最外层为8电子的稳定结构,写出其电子式________。
(3)元素①⑥能形成两种化合物,写出其中较稳定的化,合物与水反应的,离子方程式:________。
(10分)某课外实验小组利用稀硫酸与金属铁反应探究影响化学反应速率的因素,得到如下实验数据:
![]()
实验
| 铁的
| 铁的
| c/(H2SO4)
| V(H2SO4)
| 溶液温度/℃ | 金属消失
| |
反应前 | 反应后 | ||||||
1 | 0.10 | 铁片 | 0.7 | 50 | 20 | 36 | 250 |
2 | 0.10 | 铁片 | 0.8 | 50 | 20 | 35 | 200 |
3 | 0.10 | 铁粉 | 0.8 | 50 | 20 | 36 | 25 |
4 | 0.10 | 铁片 | 1.0 | 50 | 20 | 35 | 125 |
5 | 0.10 | 铁片 | 1.0 | 50 | 35 | 50 | 50 |
![]() 分析上述数据,回答下列问题:
分析上述数据,回答下列问题:
![]() (1)实验2和3表明, 对反应速率有影响,影响规律是
(1)实验2和3表明, 对反应速率有影响,影响规律是
;
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号);
(3)本实验中影响反应速率的其他因素还有 ,能体现该影响因素的实验序号是 ;
(4)在实验4中滴入几滴硫酸铜溶液,金属消失的时间小于125s。原因是
(5)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,试从反应过程能量的变化角度推测其原因 。
(10分)晶体硅是一种重要的非金属材料。请写出晶体硅的二种用途:______、______
制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅
②粗硅与干燥HCl气体反应制得SiHCl3(常温下为液态,易挥发)
③SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知:Ⅰ.SiHCl3水解会生成两种气态产物,请写出其水解的化学方程式:___________。
Ⅱ.SiHCl3 在空气中自燃。请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为 。
(2)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去)
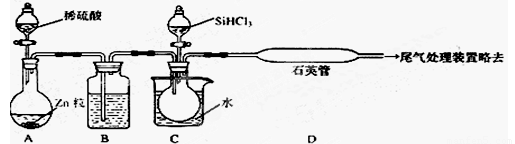
①装置B中的试剂是 ,装置C中的烧瓶需要加热,其目的是______________,
②反应一段时间后,装置D中观察到的现象是 _ ,
装置D中发生反应的化学方程式为 ___ ,
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度
以及 _____________ ,
④设计鉴定产品硅中是否含少量Fe单质的方法:_________________________________。
(10分)有一瓶浅绿色的硫酸亚铁晶体,由于保存不善,导致它在空气中敞口放置了较长的时间,因此该晶体可能被氧化。试用实验证明它是未被氧化或部分被氧化还是全部被氧化,并完成实验报告。
(1)实验目的: 。
(2)实验步骤:
①取少量该晶体溶于水,加酸酸化;
②将溶液分成两份,并置于洁净的试管中,向其中一份溶液中滴加几滴KSCN溶液;
③向另一份溶液中滴加少量的KMnO4溶液。
(2)第①步用酸酸化可以用下列的酸是
A.稀硝酸 B.盐酸 C.浓硫酸 D.稀硫酸
(3)结论:
① ,则说明部分被氧化。
② ,则说明全部被氧化。
③写出硫酸亚铁溶液在酸性条件被氧化的离子反应方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com