
题目列表(包括答案和解析)
(10分) 浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C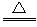 CO2↑+2H2O+2SO2↑请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
CO2↑+2H2O+2SO2↑请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
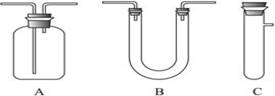
将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器(填字母) |
加入的试剂 |
作 用 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(10分)已知:溴单质(Br2)、化合物与氯的性质相似,溴单质的水溶液呈黄色,溴单质的四氯化碳溶液呈橙红色。在足量的稀氯化亚铁溶液中,加入1~2滴液态溴单质,振荡后溶液变为黄色。
⑴甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是 (填化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物质是 。
⑵现提供如下试剂:A.酸性高锰酸钾溶液B.氢氧化钠溶液C.四氯化碳D.硫氰化钾溶液实验证明乙同学的推断是正确的,请用三种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
|
|
选用试剂(代号) |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
|
第三种方法 |
|
|
⑶根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子是 。
(10分)已知:溴单质(Br2)、化合物与氯的性质相似,溴单质的水溶液呈黄色,溴单质的四氯化碳溶液呈橙红色。在足量的稀氯化亚铁溶液中,加入1~2滴液态溴单质,振荡后溶液变为黄色。
⑴甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是 (填化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物质是 。
⑵现提供如下试剂:
| A.酸性高锰酸钾溶液 | B.氢氧化钠溶液 | C.四氯化碳 | D.硫氰化钾溶液 |
| | 选用试剂(代号) | 实验现象 |
| 第一种方法 | | |
| 第二种方法 | | |
| 第三种方法 | | |
(10分) 浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C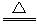 CO2↑+2H2O+2SO2↑请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
CO2↑+2H2O+2SO2↑请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)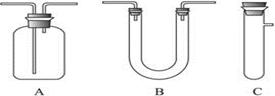
将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
| 选用的仪器(填字母) | 加入的试剂 | 作 用 |
| | | |
| | | |
| | | |
| | | |
| | | |
(本题共10分)白磷、红磷是磷的两种同素异构体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足是生成P4O10。
(1)已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)=P4O10(s) ΔH1=" -2983.2" kJ?mol-1,
P(s,红磷)+ 5/4O2(g)="1/4" P4O10(s) ΔH2=" -738.5" kJ?mol-1
则该温度下白磷转化为红磷的热化学方程式为 。
(2)已知298K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)=P4O6(s) ΔH= -1638kJ?mol-1。在某密闭容器中加入62g白磷和50.4L氧气(标准状况下),控制条件使之恰好完全反应。则所得到的P4O10和P4O6的物质的量之比为 ,反应过程中放出的热量为为 。
(3)已知白磷和PCl3的分子结构如图所示,现提供以下的化学键的键能(KJ/mol):P-P 198,Cl-Cl 243,P-Cl 331。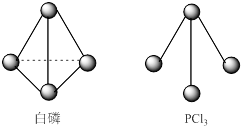
则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热ΔH = 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com