
题目列表(包括答案和解析)
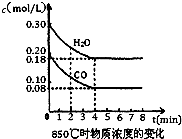 已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.
已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.| 1 | 2 |
燃料电池是燃料(例如CO、H2、CH4等)跟氧气或空气反应,将此反应的化学能转化为电能的装置,电解质通常是KOH溶液,则下列关于甲烷燃料电池的说法正确的是( )
A.负极反应式为:CH4+10OH--8e-=CO32-+7H2O
B.正极反应式为:O2+4H++4e-=2H2O
C.随着反应地进行,KOH溶液物质的量浓度不变
D.该电池的总反应与甲烷燃烧的反应方程式相同,反应式为:CH4+2O2=CO2+2H2O
燃料电池是燃料(例如CO、H2、CH4等)跟氧气或空气反应,将此反应的化学能转化为电能的装置,电解质通常是KOH溶液,则下列关于甲烷燃料电池的说法正确的是( )
| A.负极反应式为:CH4+10OH--8e-=CO32-+7H2O |
| B.正极反应式为:O2+4H++4e-=2H2O |
| C.随着反应地进行,KOH溶液物质的量浓度不变 |
| D.该电池的总反应与甲烷燃烧的反应方程式相同,反应式为:CH4+2O2=CO2+2H2O |
| 1 |
| 2 |
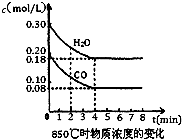
 O2(g)═H2O(l)△H2=-285.8kJ/mol
O2(g)═H2O(l)△H2=-285.8kJ/mol
1、A 2、C 3、D 4、D 5、D
6、D 7、A 8、C 9、C 10、C 11、D 12、D 13、A
14、A 15、B 16、D 17、A 18、B 19、A 20、CD 21、AC
三、非选择题
22.( 1 )①Rx 1300∽1380Ω Rx 820∽880Ω 甲
②电路图如下:
 |
 ( 2 ) ①光路图如下:
( 2 ) ①光路图如下:
② A B C
23.( 16分 )
解:依据题意,A、B均做平抛运动
以A为研究对象
xA = v0tA ① 2分
 ②
2分
②
2分
以B为研究对象
xB = v0tB ③ 1分
 ④
1分
④
1分
又由题意有  ⑤
3分
⑤
3分
由①②③④⑤式,可得
 3分
3分
代入数据: 4分
4分
24.( 18分 )
解:(1)因为带电粒子只受洛仑兹力,且洛仑兹力没有做功,所以带电粒子在磁场中的速率不变,设为V。
根据几何关系:
 ① 2分
① 2分
又粒子在磁场中匀速圆周运动洛仑兹力提供向心力,有:


 ② 2分
② 2分
 ③ 2分
③ 2分
由①②式,可得
 ④ 2分
④ 2分
(2)带电粒子从A点出发,第一次过x轴所用时间为
 ⑤
2分
⑤
2分
根据几何关系有:

联立②④式得
 ⑥
2分
⑥
2分
(3)本问不要求表述计算过程,只须写出结论:

 k=0,1,2,3…… 3分
k=0,1,2,3…… 3分

 n=0,1,2,3…… 3分
n=0,1,2,3…… 3分
25.( 20分 )
解:(1)C在B上滑动过程中,动量守恒,
 2分
2分

全过程能量守恒
 2分
2分
代入数据解得
 2分
2分
(2)AB碰撞,AB系统动量守恒
 1分
1分

AB一起运动,C在B上相对滑动
 1分
1分
 1分
1分
C滑到B的右端时,有
 2分
2分
 1分
1分
 1分
1分
代入数据有

即C在B上运动时间为
此时 
 2分
2分
此后AB分离,C在A上滑动过程中,CA系统动量守恒
 1分
1分
CA系统能量守恒
 1分
1分
 即物块C停在A上距A左端
即物块C停在A上距A左端
26.(共18分)(1)H2O
;(2)H++HSO3-=H2O+SO2↑ (3)
(4)阴; 2Cl-―2e-=Cl2↑;湿润的淀粉碘化钾试纸(其他合理答案均可给分);
27、(共12分)(1)①xCaCO3?yMgCO3 = xCaO + yMgO +(x+y) CO2↑
②CaCO3?MgCO3
(2)1:2
(3)22.4×6×ma/
28、(16分)答案:(1)分液
(2)取少量下层液体,滴入紫色石蕊试液,若颜色变红,则已有部分乙醛被氧化
(3)CH3CHO + H2SO4(浓)→
(4)①使未解聚的乙醛加合物冷凝回流 b
②溶于水,且使沸点较低的冷凝 把导管撤离锥形瓶后再熄灭酒精灯
③
29、(14分)第(1)(2)问每空2分,第(3)问每空3分]
(1) A:CH2=CH―CH2―CH2―CH=CH2
(2)C→D:酯化反应 (或取代反应) E→F:加聚反应(写聚合反应的记0分)
(3)B→C:
 |
 D→E:
D→E:
30
(一)1、五碳糖 构成核酸的成分 (每空2分,共4分)
2、复制 纺锤体 (每空2分,共4分)
3、异养型 消费者或分解者 (每空2分,共4分)
(二)
1、a.个别染色体增减; b.未受精的卵细胞发育而成 (每空3分,共6分)
2、染色体上的基因不同(或DNA分子中基因的脱氧核苷酸排列顺序不同)(4分)
31、
空腹时血糖浓度较低,蛋白质氧化供能增强,尿液中含氮物质(尿素)增多。因此可利用放射性同位素示踪法,检测尿液中的氮含量,来确定蛋白质氧化供能强度。(4分)
⑸第一步:选择生长状态、体形大小等基本一致的小鼠,饥俄一段时间使其成空腹。分A、B两组 (4分)
第二步:A组仅饲喂含14N标记的蛋白质液体,B组饲喂含14N标记的蛋白质液体和淀粉类食物 (4分)
③第三步:在一段时间后,用放射性检测仪检测两组小鼠排出的尿液中14N的含量。 (4分)
⑸①若14N在尿液中的含量A组比B组多,说明空腹时喝下的牛奶中的蛋白质主要用于氧化供能,导致营养价值降低。(或说明假设成立) (2分)
②若14N在尿液中的含量A组与B组差不多或A组比B组少,说明空腹时喝下的牛奶中的蛋白质主要用于氧化供能这个假设不成立。(或说明假设不成立) (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com