
题目列表(包括答案和解析)

| A、Na2O2晶体中阴阳离子个数比是1:1 | B、只有非金属原子之间才能形成共价键 | C、分子晶体一定含有共价键 | D、在晶体中只要有阴离子就一定有阳离子 |
根据离子晶体的晶胞(晶体中最小的重复单位),求晶体中阴阳离子个数比的方法是:?
(1)处于顶点的离子,同时为8个晶胞共有,每个离子有1/8属于晶胞?
(2)处于棱上的离子,同时为4个晶胞共有,每个离子有1/4属于晶胞?
(3)处于面上的离子,同时为2个晶胞共有,每个离子有1/2属于晶胞?
(4)处于内部的离子,则完全属于该晶胞?
现有A、B、C、D四种晶体,离子的排列方式如下图所示,其中化学式不正确的是( )
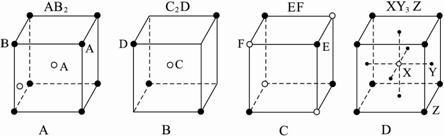
?
下列有关金属的说法正确的是
A.金属原子的核外电子在金属晶体中都是自由电子
B.体心立方晶胞和面心立方晶胞中实际含有的原子个数之比为1:2
C.金属原子在化学变化中失去的电子数越多,其还原性越强
D.金属导电的实质是金属阳离子在外电场作用下的定向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com