
题目列表(包括答案和解析)
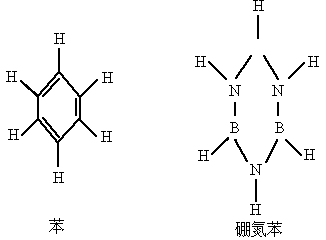
(2005·江苏)通常人们把原子总数和价电子总数相同的分子或离子称之为等电子体,等电子体间的结构相似,如化合物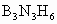 (硼氮苯)与苯是等电子体.由苯的结构和性质推测下列说法正确的是
(硼氮苯)与苯是等电子体.由苯的结构和性质推测下列说法正确的是
[ ]
A.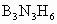 各原子不在同一平面上,是极性分子
各原子不在同一平面上,是极性分子
B.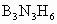 能发生加成反应和取代反应
能发生加成反应和取代反应
C.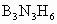 不能使酸性
不能使酸性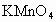 溶液褪色
溶液褪色
D.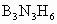 具有碱性
具有碱性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com