
题目列表(包括答案和解析)
对于2SO2(g)+O2(g) 2SO3(g) △H<0 反应来说:
2SO3(g) △H<0 反应来说:
(1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应,经2min建立平衡,此时测得SO3浓度为0.8mol·L-1,则从开始至2min用氧气表示的平均速率v(O2)= ;该条件时反应的平衡常数K= 。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有_________(填字母)。
A.升高温度 B.降低温度 C.增大压强 D.移出生成的SO3
(3)一定温度下,若将8mol SO2气体和4mol O2气体混合置于体积恒定的密闭容器中,能说明该反应已达到平衡状态的是 。
A.SO2的转化率和O2的转化率相等 B.容器内压强保持不变
C.v(SO2)逆 =" 2" v(O2)正 D.容器内密度保持不变
(4)一定温度下,将8mol SO2和4mol O2气体混合置于体积不变的密闭容器中,经t1时间达到平衡,测得混合气体总物质的量为10mol。若此时向容器中充入一定量的氦气,SO3(g)的物质的量将(填“增大”、“减小”或“不变”);若使SO2、O2、SO3三种气体均增加1mol,则平衡______________(填“向左移动”、“向右移动”或“不移动”)。
对于2SO2(g)+O2(g) 2SO3(g) △H<0 反应来说:
2SO3(g) △H<0 反应来说:
(1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应,经2min建立平衡,此时测得SO3浓度为0.8mol·L-1,则从开始至2min用氧气表示的平均速率v(O2)= ;该条件时反应的平衡常数K= 。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有_________(填字母)。
A.升高温度 B.降低温度 C.增大压强 D.移出生成的SO3
(3)一定温度下,若将8mol SO2气体和4mol O2气体混合置于体积恒定的密闭容器中,能说明该反应已达到平衡状态的是 。
A.SO2的转化率和O2的转化率相等 B.容器内压强保持不变
C.v(SO2)逆 =" 2" v(O2)正 D.容器内密度保持不变
(4)一定温度下,将8mol SO2和4mol O2气体混合置于体积不变的密闭容器中,经t1时间达到平衡,测得混合气体总物质的量为10mol。若此时向容器中充入一定量的氦气,SO3(g)的物质的量将(填“增大”、“减小”或“不变”);若使SO2、O2、SO3三种气体均增加1mol,则平衡______________(填“向左移动”、“向右移动”或“不移动”)。
对于2SO2(g)+O2(g)![]() 2SO3(g) △H<0 反应来说:
2SO3(g) △H<0 反应来说:
(1)若将2mol SO2气体和1mol O2气体在2L容器中混合并在一定条件下发生反应,经2min建立平衡,此时测得SO3浓度为0.8mol·L-1,则从开始至2min用氧气表示的平均速率v(O2)= ;该条件时反应的平衡常数K= 。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有_________(填字母)。
A.升高温度 B.降低温度 C.增大压强 D.移出生成的SO3
(3)一定温度下,若将8mol SO2气体和4mol O2气体混合置于体积恒定的密闭容器中,能说明该反应已达到平衡状态的是 。
A.SO2的转化率和O2的转化率相等 B.容器内压强保持不变
C.v(SO2)逆 = 2 v(O2)正 D.容器内密度保持不变
(4)一定温度下,将8mol SO2和4mol O2气体混合置于体积不变的密闭容器中,经t1时间达到平衡,测得混合气体总物质的量为10mol。若此时向容器中充入一定量的氦气,SO3(g)的物质的量将 (填“增大”、“减小”或“不变”);若使SO2、O2、SO3三种气体均增加1mol,则平衡______________(填“向左移动”、“向右移动”或“不移动”)。
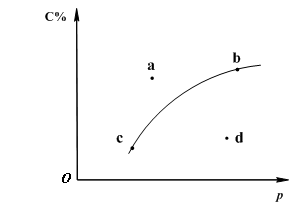
对于可逆反应2A(?)+B(g)![]() 2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
2C(g);下图是其它条件一定时反应中C的百分含量与压强的关系曲线。回答下列问题:
(1)物质A的状态是 (填“气体”、“液体”或“固体”);
(2)图-1中a、b、c、d四点中表示未达到平衡状态且v正<v逆 的点是 ;
(3)在a、b、c三种条件下达平衡时,v(a)、v(b)、v(c)按由大到小排序___________;
 |
|
(4)对于2SO2(g)+O2(g)![]() 2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
2SO3(g);ΔH=-198 kJ/mol。在实际生产过程中,原料气中SO2为7%(体积分数)、O2为11%,常压下进行,控制温度在450℃左右。
请问原料气中SO2与O2的体积比不是2∶1,而要7∶11(大约2∶3)的原因是
;如果在恒容容器中,仅把另外82%的其他气体“抽出来”,是否会减小SO2的转化率 (填“会”或“不会”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com