
题目列表(包括答案和解析)




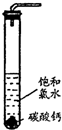 实验一、定性探究:
实验一、定性探究: HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO
HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO
HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO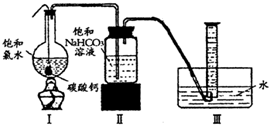
| BL |
| 22.4L/mol |
| Ag |
| 100g/mol |
下面是某同学研究氯水漂白性的一个探究性实验的片段
活动记录
[观察]氯气的颜色:黄绿色;氯水的颜色:呈黄绿色。
[结论]氯水中含有氯气分子
[实验操作]两根玻璃棒分别蘸取盐酸和氯水,各滴在两片蓝色石蕊试纸上
[实验现象]滴有盐酸的试纸变红;滴有氯水的试纸中间变白,外圈变红。
[分析与结论]氯水呈黄绿色,说明氯水中溶有游离的氯气分子。滴有氯水的蓝色石蕊试纸外圈变红,说明氯水中有能使试纸变红的酸生成;中间变白,说明氯水中有能够使有色物质褪色的物质生成。
[问题与思考]氯气溶于水发生如下反应:Cl2 + H2O = HCl +HClO,溶液中的水和盐酸都没有漂白作用,能够使有色物质褪色的物质是氯水中的氯气分子还是次氯酸呢?还是二者都有漂白作用?
请你参照某同学已完成的部分试验活动记录,自己设计一个实验,证明到底是哪种物质有漂白作用。
[实验目的]:
[实验操作]:
[实验现象]:
[分析与结论]:
[过程中用到的研究方法]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com