
题目列表(包括答案和解析)






| ||
| △ |
| ||
| △ |


| ||
| △ |
| ||
| △ |
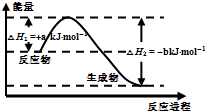 W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的一种原子的原子核中没有中子;Y与X相邻,Y与Z也相邻;X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高.试回答下列各题:
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的一种原子的原子核中没有中子;Y与X相邻,Y与Z也相邻;X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高.试回答下列各题:
| ||
| ||
一、选择题(每小题只有一个正确选项,每题2分,共50分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
A
C
C
B
B
D
D
C
B
A
C
B
D
题号
14
15
16
17
18
19
20
21
22
23
24
25
答案
D
B
A
C
D
D
C
B
D
C
D
B
二、填空题(共50分)
26、(10分)
①离子方程式为 Al(OH)3+OH-=AlO2-+2H2O ②电子式为 
③显 酸 性;原因 Al3++SH2O Al(OH)3+3H+
Al(OH)3+3H+
④化学方程式为 SO2+Cl2+2H2O=2HCl+H2SO4
⑤稳定性 HCl > H2S
27、(6分)
肯定有的离子 K+、AlO2-、CO32- ;肯定不存在的离子 NH4+、Al3+、SO42-
 是否有Cl- 有
是否有Cl- 有
 28、(10分)
28、(10分)
 (1)A
B
(1)A
B
 |

 (2)化学方程式①
(2)化学方程式①
② ③反应类型是 消去
29、(14分)
I: 制硝酸 制化肥
II: ② ④
Ⅲ:①目的 防止不钝的氢气加热不安全
②现象是 固液脱离接触
原因是 以大氢气的浓度提高N2转化率
气体成分是 N2、H2
③原因是 铁触媒在较高温度时活性大,加快氨合成速率
化学方程式 
四、计算题(共10分)
30、(10分)
 ①
① 
② 0.025
③ 0.005 0.005
④ 0.005mkx<0.015ml
 天星教育网(www.tesoon.com) 版权所有
天星教育网(www.tesoon.com) 版权所有
天星教育网(www.tesoon.com) 版权所有
天星教育网(www.tesoon.com) 版权所有
|