
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
| ‘™Àÿ –‘÷ |
¢Ÿ |
¢⁄ |
¢€ |
¢Ð |
¢ð |
¢Þ |
¢þ |
¢ý |
¢· |
¢‚ |
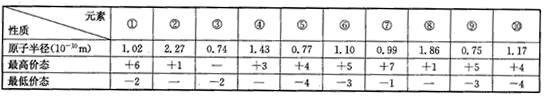
| ‘≠◊”∞Îæ∂ £®10-10m£© |
1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| ◊Ó∏þº€Ã¨ | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| ◊ÓµÕº€Ã¨ | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
 £®I£©µŒ∂®∑÷Œˆ∑® «ªØ—ß∑÷Œˆ∑®÷–µƒ÷ÿ“™∑÷Œˆ∑Ω∑®÷Æ“ª£Æ
£®I£©µŒ∂®∑÷Œˆ∑® «ªØ—ß∑÷Œˆ∑®÷–µƒ÷ÿ“™∑÷Œˆ∑Ω∑®÷Æ“ª£Æ| µŒ∂®¥Œ ˝ µ—È ˝æð£®mL£© |
1 | 2 | 3 | 4 |
| V£®—˘∆∑£© | 20.00 | 20.00 | 20.00 | 20.00 |
| V£®NaOH£©£®œ˚∫ƒ£© | 15.95 | 15.00 | 15.05 | 14.95 |

| µ—È≤Ω÷Ë | µ—Èœ÷œÛ | µ—ÈΩ·¬€ | |
| µ—È“ª | Ω´¥¯ª–«µƒƒæÃı…Ï»Î◊∞”–π˝—ıªØ«‚»Ð“∫µƒ ‘πÐ÷– | ƒæÃı≤ª∏¥»º | ≥£Œ¬œ¬π˝—ıªØ«‚»Ð“∫≤ª∑÷Ω‚£®ªÚ∑÷Ω‚∫Ð…Ÿ£© £ø £ø |
| µ—È∂˛ | ‘⁄◊∞”–H2O2»Ð“∫µƒ ‘πÐ÷–º”»Î…Ÿ¡øAl2O3£¨»ª∫ÛΩ´¥¯ª–«µƒƒæÃı…ϻΠ‘πÐ÷– | ƒæÃı∏¥»º | Al2O3ƒÐº”øÏH2O2»Ð“∫µƒ∑÷Ω‚ÀŸ¬ Al2O3ƒÐº”øÏH2O2»Ð“∫µƒ∑÷Ω‚ÀŸ¬ |

≤ðÀ· «“ª÷÷÷ÿ“™µƒ ‘º¡°£œ¬√Ê «¿˚”√≤ðÀ·ÃΩæø≈®∂»∂‘∑¥”¶ÀŸ¬ ”∞œÏµƒ µ—È°£
£®1£©Œ™÷§√˜≈®∂»∂‘∑¥”¶ÀŸ¬ µƒ”∞œÏ£¨‘¯”–ΩÃø∆ È°∂ªØ—ß∑¥”¶‘≠¿Ì°∑…˺∆¡À»Áœ¬ µ—È£∫»°¡Ω÷ß ‘πУ¨∏˜º”»Î4mL0.01mol°§L-1µƒKMnO4À·–‘»Ð“∫£¨∑÷±œÚ∆‰÷–º”»Î0.1 mol°§L-1°¢0.2 mol°§L-1 H2C2O4»Ð“∫2mL£¨º«¬º»Ð“∫Õ …´À˘–Ë ±º‰°£
µ—È÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™£∫ £ª
‘§∆⁄œ÷œÛ «£∫
¢Ÿ»Ð“∫µƒ—’…´”… …´±‰Œ™ …´£¨
¢⁄∆‰÷–º”»Î mol°§L-1H2C2O4µƒƒ«÷ß ‘πÐ÷–µƒ»Ð“∫œ»±‰…´°£
»ª∂¯ µ—ÈΩ·π˚≤¢≤ªæ°»Á»À“‚°£ µ—Èπ˝≥×’…´∏¥‘”£¨«“Õ …´œ»ª∫¬˝£¨∫Û÷Ω•º”øÏ£ª◊Ó¥ÛµƒŒ  «≤ðÀ·≈®∂»¥Û£¨∑¥”¶ÀŸ¬ »¥∏¸¬˝°£
±æ µ—ȃÐ∑Ò◊˜Œ™øŒÃ√ µ—È—–æø≈®∂»∂‘ªØ—ß∑¥”¶ÀŸ¬ µƒ”∞œÏ£ø “ÀµƒÃıº˛ «‘ı—˘µƒ£øƒ≥–£“ª—–æø–°◊È∂‘¥ÀΩ¯––¡ÀÃΩæø°£œ¬√Ê «À˚√«µƒ µ—ȱ®∏ʵƒ“ª≤ø∑÷£∫
±Ì1°° ‘—È∞≤≈≈º∞Ω·π˚
|
µ—È ±ý∫≈ |
A£®KMnO4»Ð“∫≈®∂»/mol°§L-1£© |
B£®≤ðÀ·»Ð“∫≈®∂»/mol°§L-1£© |
C£®¡ÚÀ·»Ð“∫≈®∂»/mol°§L-1£© |
Õ …´ ±º‰/s |
|
1 |
3 |
3 |
1 |
336 |
|
2 |
1 |
2 |
3 |
82 |
|
3 |
3 |
1 |
3 |
76 |
|
4 |
1 |
3 |
2 |
133 |
|
5 |
2 |
3 |
3 |
102 |
|
6 |
3 |
2 |
2 |
156 |
|
7 |
2 |
2 |
1 |
300 |
|
8 |
2 |
1 |
2 |
115 |
|
9 |
1 |
1 |
1 |
200 |
”¶”√SPSS16.0∂‘’˝Ωª ‘—ÈΩ·π˚Ω¯––∑Ω≤Ó∑÷Œˆ£¨Ω·π˚»Áœ¬±Ì
±Ì2°°∏˜“ÚÀÿÀÆ∆Ωµƒ ˝æ𥶿ÌΩ·π˚
|
|
A£®KMnO4»Ð“∫£© |
B£®≤ðÀ·»Ð“∫£© |
C£®¡ÚÀ·»Ð“∫£© |
||||||
|
≈®∂»/mol°§L-1 |
0.005 |
0.010 |
0.015 |
0.1 |
0.5 |
0.9 |
6 |
12 |
18 |
|
∆Ωæ˘Õ …´ ±º‰/s |
138.3 |
172.3 |
189.3 |
130.3 |
179.3 |
190.3 |
278.7 |
134.7 |
86.7 |
£®2£©”…±Ì2ø…÷™£¨»˝“ÚÀÿ÷–£¨ µƒ≈®∂»£®—°ÃÓ°∞A°¢BªÚC°±£¨œ¬ø’Õ¨£©∂‘∑¥”¶ÀŸ¬ ”∞œÏœ‘÷¯£¨∂¯ µƒ≈®∂»∂‘∑¥”¶ÀŸ¬ µƒ”∞œÏ≤ªœ‘÷¯°£
£®3£©”…±Ì2ø…÷™£¨µ±∏þ√ÃÀ·ºÿ≈®∂»Œ™ mol°§L-1°¢≤ðÀ·≈®∂»Œ™ mol°§L-1 ±£¨∑¥”¶◊ÓøÏ°£º¥“ÚÀÿA°¢BµƒΩœ “À µ—ÈÃıº˛µ√“‘»∑∂®°£
∏˘æð“‘…œ µ—ÈΩ·π˚£¨∏√–°◊ÈÕ¨—ߺÖ¯ÃΩæø¡ÚÀ·µƒ≈®∂» «‘ı—˘”∞œÏ±æ∑¥”¶ÀŸ¬ µƒ£¨≤‚µ√»Áœ¬ µ—ÈΩ·π˚£∫
±Ì3°°≤ªÕ¨¡ÚÀ·≈®∂»œ¬µƒÕ …´ ±º‰
|
c(H2SO4)/mol°§L-1 |
18 |
16 |
14 |
12 |
10 |
8 |
6 |
|
Õ …´ ±º‰/s |
67 |
83 |
90 |
103 |
129 |
146 |
200 |
£®4£©∏˘æðøŒÃ√ µ—ȵƒ∫œ ±º‰£¨ø…—°»Ð“∫µƒÕ …´ ±º‰‘ºŒ™1∑÷÷”∫Õ2∑÷÷”µƒ¡Ω∑ð»Ð“∫£¨º¥¥À ±¡ÚÀ·µƒ≈®∂»Œ™ mol°§L-1∫Õ mol°§L-1£¨’‚“≤”–¿˚”⁄π€≤Ï’‚¡Ω∏ˆ∑¥”¶ÀŸ¬ µƒ≤Ó“Ï°£
Ω·¬€£∫≤ðÀ·”ÎÀ·–‘∏þ√ÃÀ·ºÿ»Ð“∫µƒ∑¥”¶£¨ø…◊˜Œ™øŒÃ√ µ—ÈÃΩæø≈®∂»∂‘∑¥”¶ÀŸ¬ µƒ”∞œÏ°£
| µŒ∂®¥Œ ˝ µ—È ˝æð£®mL£© | 1 | 2 | 3 | 4 |
| V£®—˘∆∑£© | 20.00 | 20.00 | 20.00 | 20.00 |
| V£®NaOH£©£®œ˚∫ƒ£© | 15.95 | 15.00 | 15.05 | 14.95 |

| µ—È≤Ω÷Ë | µ—Èœ÷œÛ | µ—ÈΩ·¬€ | |
| µ—È“ª | Ω´¥¯ª–«µƒƒæÃı…Ï»Î◊∞”–π˝—ıªØ«‚»Ð“∫µƒ ‘πÐ÷– | ƒæÃı≤ª∏¥»º | ≥£Œ¬œ¬π˝—ıªØ«‚»Ð“∫≤ª∑÷Ω‚£®ªÚ∑÷Ω‚∫Ð…Ÿ£©______ |
| µ—È∂˛ | ‘⁄◊∞”–H2O2»Ð“∫µƒ ‘πÐ÷–º”»Î…Ÿ¡øAl2O3£¨»ª∫ÛΩ´¥¯ª–«µƒƒæÃı…ϻΠ‘πÐ÷– | ƒæÃı∏¥»º | ______ |


π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com