
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
£Ø12·Ö£©Ä³Š£»Æѧъ¾æŠ”×éµÄĶ¬Ń§ŅŃÖŖĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄʵĻÆѧŠŌÖŹ£¬²¢¶ŌĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄȵĻīĘĆŠŌ½ųŠŠĮĖČēĻĀŹµŃéĢ½¾æ£ŗ
I”¢ĪŖĮĖ¼ų±šĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄĘĮ½ÖÖ°×É«¹ĢĢ壬Š”×é³ÉŌ±ÓĆ²»Ķ¬µÄ·½·Ø½ųŠŠĮĖŹµŃ飬ČēĻĀĶ¼×°ÖĆĖłŹ¾£ŗ
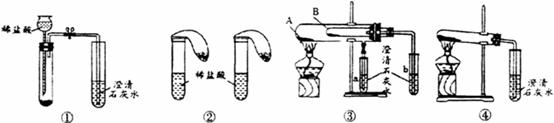
(1)Ö»øł¾ŻĶ¼¢Ł”¢Ķ¼¢ŚĖłŹ¾ŹµŃ飬Äܹ»Ć÷Č·“ļµ½ŹµŃéÄæµÄµÄŹĒ_______£ØĢī”°¢Ł”±»ņ ”°¢Ś”±£©
(2)ČōÓĆĶ¼¢ŪĖłŹ¾ŹµŃé×°ÖĆŃéÖ¤Ģ¼ĖįÄʱČĢ¼ĖįĒāÄʵÄĪČ¶ØŠŌŗĆ£¬ŌņĢ¼ĖįĒāÄĘӦװČė_________¹ÜÖŠ£ØĢī”°A”±»ņ”°B”±£©”£
(3)ÓŠĶ¬Ń§Ģį³öÓĆĶ¼¢ÜĖłŹ¾ŹµŃé×°ÖĆ¾ĶÄÜŌŚŅ»“ĪŹµŃ锢Ņ»øö·“Ó¦ÖŠ±Č½Ļ³öĢ¼ĖįÄĘŗĶĢ¼ĖįĒāÄʵÄČČĪČ¶ØŠŌĻą¶ŌĒæČõ£¬ÄćČĻĪŖÕāøöĖµ·Ø___________£ØĢī”°ÕżČ·”±»ņ”°²»ÕżČ·”±£©
¢ņ”¢ŅŃÖŖ£ŗ10”ꏱ£¬ŌŚÉÕ±ÖŠ¼ÓČė![]() µÄ
µÄ![]() ČÜŅŗ400mL£¬²āµĆøĆČÜŅŗŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄpH£Ø¼ūĻĀ±ķ£©£ŗ
ČÜŅŗ400mL£¬²āµĆøĆČÜŅŗŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄpH£Ø¼ūĻĀ±ķ£©£ŗ
| ĪĀ¶Č£Ø”ę£© | 10 | 20 | 30 | 50 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 |
¼×Ķ¬Ń§½«![]() µÄ
µÄ![]() ČÜŅŗÖĆÓŚÉÕ±ÖŠ¼ÓČČÖĮ50”ę£¬²āĘäpHĪŖ8.9£»ŌŁ½«ČÜŅŗĄäČ“ÖĮ20”ę£¬²āĘäpHČŌĪŖ8.4”£ŅŅĶ¬Ń§½«200mL”¢20”ę”¢
ČÜŅŗÖĆÓŚÉÕ±ÖŠ¼ÓČČÖĮ50”ę£¬²āĘäpHĪŖ8.9£»ŌŁ½«ČÜŅŗĄäČ“ÖĮ20”ę£¬²āĘäpHČŌĪŖ8.4”£ŅŅĶ¬Ń§½«200mL”¢20”ę”¢
![]() µÄ
µÄ![]() ČÜŅŗÖĆÓŚÉÕ±ÖŠ¼ÓČČÖĮ90”ęŅ»¶ĪŹ±¼äŗ󣬽«ČÜŅŗĄäČ“ÖĮ
ČÜŅŗÖĆÓŚÉÕ±ÖŠ¼ÓČČÖĮ90”ęŅ»¶ĪŹ±¼äŗ󣬽«ČÜŅŗĄäČ“ÖĮ
20”ę£¬²āĘäpHĪŖ10.1£ØČÜŅŗĢå»ż²»±ä£©”£
Ēė¶ŌÉĻŹöŹµŃéĻÖĻó×÷³öĖµĆ÷”£
£Ø10·Ö£©ŅŃÖŖAĪŖ֊ѧ»Æѧ֊µÄŅ»ÖÖŃĪ£¬B”¢CĪŖČÕ³£Éś»īÖŠ³£¼ūµÄ½šŹō”£Ķس£
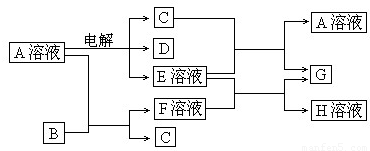
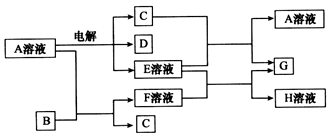
Ģõ¼žĻĀDĪŖĪŽÉ«ĪŽĪ¶ĘųĢ壬ĪŽÉ«ĘųĢåGÓöæÕĘų±äŗģ×ŲÉ«”£ŅŃÖŖÓƶčŠŌµē¼«µē½āAČÜŅŗŅ»¶ĪŹ±¼äŗ󣬲śĪļÖ»ÓŠC”¢DŗĶEµÄĻ”ČÜŅŗ”£ø÷ĪļÖŹÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĻĀĶ¼£Ø²æ·Ö·“Ó¦²śĪļŅŃĀŌČ„£©”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄ»ÆѧŹ½ĪŖ ”£
£Ø2£©AČÜŅŗÓėNa2O2·“Ó¦µÄ×Ü»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø3£©EµÄĻ”ČÜŅŗÓėFČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø4£©µē½ā100mLŃĪAµÄČÜŅŗŅ»¶ĪŹ±¼äŗ󣬶ĻæŖµēĀ·£¬Č”³öµē¼«£¬²āµĆĖłµĆµ½µÄĘųĢåDŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ5.6mL£¬Ōņµē½āŗóČÜŅŗµÄpHĪŖ ”££Ø¼ŁÉčČÜŅŗĢå»ż²»±ä£©
£Ø5£©ČōĻņ100mLŃĪAµÄČÜŅŗÖŠ¼ÓČė10g½šŹōµ„ÖŹBµÄ·ŪÄ©£¬³ä·Ö½Į°čŗ󣬹żĀĖ£¬ŗęøɵĆ10.16g¹ĢĢ壬ŌņĀĖŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæÅضČĪŖ ”££Ø¼ŁÉčČÜŅŗĢå»ż²»±ä£©
£Ø10·Ö£©ŅŃÖŖAĪŖ֊ѧ»Æѧ֊µÄŅ»ÖÖŃĪ£¬B”¢CĪŖČÕ³£Éś»īÖŠ³£¼ūµÄ½šŹō”£Ķس£
Ģõ¼žĻĀDĪŖĪŽÉ«ĪŽĪ¶ĘųĢ壬ĪŽÉ«ĘųĢåGÓöæÕĘų±äŗģ×ŲÉ«”£ŅŃÖŖÓƶčŠŌµē¼«µē½āAČÜŅŗŅ»¶ĪŹ±¼äŗ󣬲śĪļÖ»ÓŠC”¢DŗĶEµÄĻ”ČÜŅŗ”£ø÷ĪļÖŹÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĻĀĶ¼£Ø²æ·Ö·“Ó¦²śĪļŅŃĀŌČ„£©”£

Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄ»ÆѧŹ½ĪŖ ”£
£Ø2£©AČÜŅŗÓėNa2O2·“Ó¦µÄ×Ü»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø3£©EµÄĻ”ČÜŅŗÓėFČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø4£©µē½ā100mLŃĪAµÄČÜŅŗŅ»¶ĪŹ±¼äŗ󣬶ĻæŖµēĀ·£¬Č”³öµē¼«£¬²āµĆĖłµĆµ½µÄĘųĢåDŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ5.6mL£¬Ōņµē½āŗóČÜŅŗµÄpHĪŖ ”££Ø¼ŁÉčČÜŅŗĢå»ż²»±ä£©
£Ø5£©ČōĻņ100mLŃĪAµÄČÜŅŗÖŠ¼ÓČė10g½šŹōµ„ÖŹBµÄ·ŪÄ©£¬³ä·Ö½Į°čŗ󣬹żĀĖ£¬ŗęøɵĆ10.16g¹ĢĢ壬ŌņĀĖŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæÅضČĪŖ ”££Ø¼ŁÉčČÜŅŗĢå»ż²»±ä£©
Ņ»”¢ Ń”ŌńĢā£Ø±¾Ģā°üĄØ15Š”Ģā£¬Ć抔ĢāÖ»ÓŠŅ»øöŃ”Ļī·ūŗĻĢāŅā£¬ĆæĢā4·Ö£¬¹²60·Ö£©
1 D 2. D 3. B 4. C 5. D 6. D 7.B 8. D 9. C
10 .B
¶ž”¢Ń”ŌńĢā
16 AD 17 D 18D
”¾±Ų×ö²æ·Ö”æ
23.£Ø12·Ö£©£Ø1£©Ķ¼ÕżČ·µĆ2·Ö
£Ø2£©µēŃ¹UÓėµē×čRµÄ±ČÖµ£Ø»ņµēĮ÷I£©£Ø2·Ö£©£ŗ±ķøńÖŠø÷µēĮ÷Öµ·Ö±šĪŖ0.05£¬0.09£¬0.14£¬0.20£¬0.24£¬0.27£Ø2·Ö£©£»Ķ¼ĻńČēĶ¼ĖłŹ¾£Ø2·Ö£©
£Ø3£©2.00£Ø1.98ØD2.02£©£Ø2·Ö£©,0.45(0.40ØD0.50) £Ø2·Ö£©

24.£Ø15·Ö£©½ā£ŗ£Ø1£©ŌĖ¶ÆŌ±“Ó×īøßµćĻĀĀä¹ż³ĢĪŖĘ½Å×ŌĖ¶Æ£¬ŹśÖ±·ÖŌĖ¶ÆĪŖ×ŌÓÉĀäĢåŌĖ¶Æ”£ÉčŌĖ¶ÆŌ±ĘšĢųŗóÖŲŠÄĄėµŲµÄø߶ČĪŖH,Ōņ
 £Ø2·Ö£©
£Ø2·Ö£©
¼“ £Ø2·Ö£©
£Ø2·Ö£©
£Ø2£©ÉčŌĖ¶ÆŌ±½ÅøÕ“„µŲŹ±µÄŹśÖ±·ÖĖŁ¶ČĪŖ ”£ŌņÓÉ»śŠµÄÜŹŲŗć£¬
”£ŌņÓÉ»śŠµÄÜŹŲŗć£¬
 £Ø4·Ö£©
£Ø4·Ö£©
ÉčŌĖ¶ÆŌ±ĀäµŲŹ±ŹÜµ½µÄŹśÖ±·½ĻņµÄĘ½¾ł×÷ÓĆĮ¦ĪŖF,ÓɶÆÄÜ¶ØĄķµĆ

 £Ø4·Ö£©
£Ø4·Ö£©
ĮŖĮ¢Į½Ź½µĆ £Ø3·Ö£©
£Ø3·Ö£©
25.£Ø18·Ö£©½ā£ŗ£Ø1£©Į£×ÓŌŚµŚŅ»ĻóĻŽ×öĄąĘ½Å×ŌĖ¶Æ£¬
¼ÓĖŁ¶Č £Ø3·Ö£©
£Ø3·Ö£©
ŌĖ¶ÆŹ±¼ä  £Ø2·Ö£©
£Ø2·Ö£©
ŃŲ ·½ĻņµÄĪ»ŅĘ
·½ĻņµÄĪ»ŅĘ
£Ø2£©Į£×ÓĶعż Öį½ųČė“ų”Ź±ŌŚ
Öį½ųČė“ų”Ź±ŌŚ ·½ĻņÉĻµÄĖŁ¶Č
·½ĻņÉĻµÄĖŁ¶Č
 £Ø2·Ö£©
£Ø2·Ö£©
Ņņ“Ė
Į£×ÓŌŚµŚ¶žĻóĻŽŅŌ ĪŖŌ²ŠÄ×öŌČĖŁŌ²ÖÜŌĖ¶Æ£¬Ō²»”Ėł¶ŌµÄŌ²ŠÄ½ĒĪŖ
ĪŖŌ²ŠÄ×öŌČĖŁŌ²ÖÜŌĖ¶Æ£¬Ō²»”Ėł¶ŌµÄŌ²ŠÄ½ĒĪŖ £¬ŌĖ¶ÆŹ±¼ä
£¬ŌĖ¶ÆŹ±¼ä

£Ø3£©Į£×ӓӓų”·µ»Ųµē³”ŗóµÄŌĖ¶ÆŹĒ“ĖĒ°Óɵē³”½ųČė“ų”ŌĖ¶ÆµÄÄęŌĖ¶Æ£¬¾Ź±¼ä
Į£×ÓµÄĖŁ¶Č±äĪŖ £¬“ĖŗóÖŲø“Ē°ĆęµÄŌĖ¶Æ”££Ø2·Ö£©
£¬“ĖŗóÖŲø“Ē°ĆęµÄŌĖ¶Æ”££Ø2·Ö£©
Į£×ÓŌŚµē“ų”ÖŠŌĖ¶ÆµÄÖÜĘŚ £Ø2·Ö£©
£Ø2·Ö£©
26. £Ø15·Ö£©
£Ø1£©³¢ X ¼×²”ÄŠÅ®»¼ÕßČĖŹż»ł±¾ĻąĶ¬£¬ŅŅ²”ÄŠŠŌ»¼Õ߶ąÓąÅ®ŠŌ»¼ÕߣØ2·Ö£© »łŅņĶ»±ä£Ø2£©¢ŁaaXbY aaXBXb »ņaaXBXb £Ø²»Č«²»øų·Ö£©
¢Ś 1/2 ¢Ū 1/2 1/16 Å®
£Ø3£©Ōö¼Ó ±ķŠÖĆĆÖ®¼äÓŠŅ»²æ·Ö»łŅņĻąĶ¬£ØŠÆ“ųĶ¬ÖÖŅžŠŌÖĀ²”»łŅņµÄæÉÄÜŠŌ½Ļ“ó£©
£Ø4£©ŅÅ“«×ÉŃÆ£¬²śĒ°Õļ¶Ļ£Ø2·Ö£©
27£Ø18·Ö£©£Ø1£©Éń¾-ĢåŅŗ”¢ĆāŅߣØ2·Ö£© ŗ¬ĮæÉŁ”¢×÷ÓĆ“ó£Ø2·Ö£©
£Ø2£©I ŅȵŗĖŲ£Ø1·Ö£© ŃŖĢĒĄūÓĆ”¢×Ŗ»ÆĪŖĢĒŌŖ£Ø2·Ö£© ·ĒĢĒĪļÖŹ×Ŗ»ÆĪŖŃŖĢĒ£ØøĪĢĒŌŖµÄ·Ö½ā£©£Ø2·Ö£©
II ·“Ą”µ÷½Ś£Ø2·Ö£©
III Ļø°ūĤÉĻŹÜĢåµ°°×²»Õż³££Ø»ņa¼¤ĖŲ²»ÄÜÓėŹÜĢå½įŗĻ»ņæŲÖĘ Ļø°ūĤÉĻŹÜĢåµ°°×µÄ»łŅņ·¢ÉśĶ»±äĖłÖĀ£©ĘäĖūŗĻĄķ“š°øŅąøų·Ö”££Ø3·Ö£©
 £Ø3£©¼ūĻĀĶ¼£¬ĆæĶ¼2·Ö£¬¹²4·Ö
£Ø3£©¼ūĻĀĶ¼£¬ĆæĶ¼2·Ö£¬¹²4·Ö
28.£Ø16·Ö£©
£Ø1£©Cu2S£Ø2·Ö£© £Ø2£©Cu2S£Ø2·Ö£©15mol£Ø2·Ö£©
£Ø3£©ĖįÓźÖŠÖ÷ŅŖ³É·ÖĪŖH2SO3 £ŗSO2-H2O=2H2SO2 £Ø1·Ö£© H2SO3ŌŚæÕĘųÖŠ±»Ńõ»Æ£ŗ
2H2SO3+O2=2H2SO4 £Ø1·Ö£© ĮņĖįµÄĖįŠŌ±ČŃĒĮņĖįĒæ£Ø1·Ö£©
£Ø4£©CuCO3?Cu(OH)2+4H£=2Cu2++3 H2O+CO2 £Ø2·Ö£©
£Ø5£©·ń £Ø1·Ö£© Cu+2Fe3+= Cu2++2 Fe2+ £Ø2·Ö£© ĀČĖ®£Ø»ņĖ«ŃõĖ®£© £Ø2·Ö£©
29. £Ø14·Ö£©
£Ø1£©0.1 £Ø3·Ö£© £Ø2£©a £Ø3·Ö£©
£Ø3£©¢Ł·“Ó¦¢Ł £Ø2·Ö£© Fe(OH)3+5OH-+3e-=Fe +4H2O
£Ø3·Ö£©
+4H2O
£Ø3·Ö£©
¢ŚĒæŃõ»ÆŠŌÄÜɱ¾śĻū¶¾£¬Ę仹Ō²śĪļFe3-Ė®½ā[Fe3-+3H2O=Fe(OH)3(½ŗĢå)+3H-Éś³ÉFe(OH)3½ŗĢåÄÜĪüø½Ė®ÖŠŌÓÖŹ³Į½µ¶ų¾»Ė®£Ø3·Ö£©
30. £Ø12·Ö£©
I £Ø1£©¢Ś£Ø2·Ö£© £Ø2£©B £Ø2·Ö£© £Ø3£©ÕżČ·£Ø2·Ö£©
II “Ó¼×”¢ŅŅĮ½Ķ¬Ń§ŹŌŃéæÉŅŌ擳ö£»
¢Ł ¼ÓČČĢ¼ĖįĒāÄĘČÜŅŗÖĮ Ąė×ÓĖ®½ā£¬Ź¹ČÜŅŗ¼īŠŌŌöĒæ£Ø3·Ö£©
Ąė×ÓĖ®½ā£¬Ź¹ČÜŅŗ¼īŠŌŌöĒæ£Ø3·Ö£©
¢Ś µ±¼ÓČČĢ¼ĖįĒāļ§ČÜŅŗÖĮ
31.ĀŌ
32.£Ø¹²8·Ö£©
£Ø1£©1 £Ø1·Ö£© 2 £Ø1·Ö£© £¬Čż½Ē׶ŠĪ£Ø1·Ö£©
£Ø2£©µĶÓŚ£Ø1·Ö£© Cl2¾§ĢåŹōÓŚ·Ö×Ó¾§Ģ壬Si¾§ĢåŹōÓŚŌ×Ó¾§Ģ壬Ō×Ó¾§ĢåÖŠŌ×ÓÖ®¼äŅŌŗÜĒæµÄ¹²¼Ū¼ü½įŗĻ£¬¶ų·Ö×Ó¾§ĢåÖŠ·Ö×Ó¼äŅŌ½ĻČõµÄ·Ö×Ó¼ä×÷ÓĆĮ¦½įŗĻ£¬Ņņ¶ųŌ×Ó¾§ĢåµÄČŪµć±Č·Ö×Ó¾§ĢåµÄČŪµćøߣØ2·Ö£©
£Ø3£©1s22s22p63s23p64s13d5£Ø2·Ö£©
33.(8·Ö)

£Ø3£©Ńõ»Æ·“Ó¦ £Ø2·Ö£©
34. (8·Ö) £Ø1£©
£Ø3£©½ŗʬÉĻµÄµ°°×Ĥ“ęŌŚŹ±¼äµÄ³¤¶Ģ£Ø»ņĘäĖūĄķÓÉ“š°ø£© £Ø4£©¹Ģ¶Ø»ÆĆø
£Ø5£©ŻĶČ”·Ø”¢ÕōĮó·Ø”¢Ń¹Õ„·Ø£ØÖ»ŅŖ“š³ö2Ģõ£¬¾ĶµĆ2·Ö£©
£Ø6£©Ę½°å»®Ļß·Ø Ļ”ŹĶĶæ²¼Ę½°å·Ø
35. (8·Ö) £Ø1£©ŗĖŅĘÖ²¼¼Źõ”¢¶ÆĪļĻø°ūÅąŃų£ØȱŅ»²»øų·Ö£©
£Ø2£©»łŅņĪÄæāÖŠĢįČ”£¬PCR¼¼ŹõĄ©Ōö£¬ČĖ¹¤»ÆѧŗĻ³É£ØÖĮÉŁ“š¶Ō2Ļī²ÅÄÜµĆ·Ö£©Ęō¶Æ×Ó”¢ÖÕÖ¹×Ó”¢±ź¼Ē»łŅņ£ØȱŅ»²»øų·Ö£© ĻŌĪ¢×¢Éä·Ø
£Ø3£©Ņȵ°°×Ćø»ņ½ŗŌµ°°×Ćø ¼õŹżµŚ¶ž“Ī·ÖĮŃÖŠĘŚ
£Ø4£©É£ ÅßŗĶÄŅÅß ½ŚŌ¼×ŹŌ“”¢½µµĶ³É±¾µČ£Ø×ĆĒéøų·Ö£©
ÅßŗĶÄŅÅß ½ŚŌ¼×ŹŌ“”¢½µµĶ³É±¾µČ£Ø×ĆĒéøų·Ö£©
36. (8·Ö)
£Ø1£©  £Ø1·Ö£©
£Ø1·Ö£©  £Ø1·Ö£©
£Ø1·Ö£©
£Ø2£©¢Ł»īČū»ŗĀżĻĀŅĘ£¬ĄķĻėĘųĢåĪĀ¶Č²»±ä£¬ÄŚÄܲ»±ä£¬Ģå»ż¼õŠ”£¬Ķā½ē¶ČĘųĢå×ö¹¦£¬øł¾ŻČČĮ¦Ń§µŚŅ»¶ØĀÉÖŖ£¬ĘųĢå·ÅČČ”££Ø2·Ö£©
¢Śøł¾Ż²£Ņā¶ś¶ØĀÉ£ŗ £Ø2·Ö£©
£Ø2·Ö£©
»īČūŅʶÆŗóĘųĢåµÄĢå»żĪŖ£ŗ £Ø2·Ö£©
£Ø2·Ö£©
37. (8·Ö)
½ā£ŗ£Ø1£©“«²„ĖŁ¶Č  £Ø2·Ö£©
£Ø2·Ö£©
£Ø2£©²ØÓɲØŌ““«µ½JĖłŠčŹ±¼ä £Ø1·Ö£©
£Ø1·Ö£©
²ØøÕ“«µ½JµćŹ±£¬JĻņÉĻŌĖ¶Æ£¬µ½øŗµÄ×ī“óĪ»Ņʊ菱 £Ø1·Ö£©
£Ø1·Ö£©
ĖłŅŌ×ÜŹ±¼äĪŖ £Ø1·Ö£©
£Ø1·Ö£©
£Ø3£©Ķ¼3·Ö

38. (8·Ö)
£Ø1£© 2£Ø1·Ö£© ÖŹ×ӣػņ £© £Ø1·Ö£© ;
£© £Ø1·Ö£© ; £Ø2·Ö£©
£Ø2·Ö£©
£Ø2£©Éč¼ÓĖŁŗóŗ½ĢģĘ÷µÄĖŁ¶Č“óŠ”ĪŖ £¬ÓɶÆĮæŹŲŗć¶ØĀÉÓŠ
£¬ÓɶÆĮæŹŲŗć¶ØĀÉÓŠ
 £Ø3·Ö£©
£Ø3·Ö£©
 £Ø1·Ö£©
£Ø1·Ö£©
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com