
题目列表(包括答案和解析)
原高中教材中有这样一个实验:在两支试管中分别加入3 mL稀盐酸,将两个各装有0.3 g NaHCO3或Na2CO3粉末的小气球分别套在两支试管口,将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下:
(1)两支试管均产生大量气体,投入________的试管中气体产生较快,投入________的试管中气球变得更大(以上均填化学式).
(2)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度有升高.由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应.甲同学写出了下列热化学方程式(其中“aq”的含义是表示水溶液):
HCOCO![]() (aq)+2H+(aq)=H2O(l)+CO2(g)△H<0
(aq)+2H+(aq)=H2O(l)+CO2(g)△H<0
甲下结论的方法是否正确________(填“正确”或“不正确”);为研究是吸热还是放热反应,乙同学继续进行了下列实验(每次实验各做3次平行实验,取平均值):
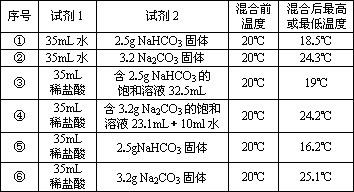
请你帮助填写相关内容:
该研究报告的题目可拟为《________》
通过上述实验可得出四条结论:
①NaHCO3的溶解是________(填“吸热”或“放热”)过程;
②Na2CO3的溶解是________(填“吸热”或“放热”)过程;
③NaHCO3的饱和溶液和盐酸的反应是________(填“吸热”或“放热”)反应;
④Na2CO3的饱和溶液和盐酸的反应是________(填“吸热”或“放热”)反应.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com